Recherche et Statistiques en Psychologie, Neurosciences et Comportement Copyright © 2024 by Ali Hashemi is licensed under a Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License, except where otherwise noted.
Recherche et Statistiques en Psychologie, Neurosciences et Comportement Copyright © 2024 by Ali Hashemi is licensed under a Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License, except where otherwise noted.
1
Bienvenue sur RS en PNC ! Il s’agit d’une ressource électronique ouverte (REL) conçue pour vous aider à comprendre les statistiques pour une variété de disciplines psychologiques différentes en utilisant des données simulées basées sur des recherches réelles. Après tout, un aspect fondamental de la recherche en psychologie est la connaissance des statistiques.
Vous avez peut-être remarqué que les programmes de psychologie de premier cycle comprennent presque toujours au moins un cours sur l’utilisation des statistiques dans la recherche psychologique et, peut-être à votre grand désarroi, votre instructeur peut vous demander d’utiliser le logiciel statistique R pour faire vos devoirs et vos tests. Vous ne serez probablement pas surpris d’apprendre que l’apprentissage de R n’est pas facile (ou du moins pas aussi facile que nous le souhaiterions) pour de nombreux étudiants. Cela peut avoir un impact direct sur l’incapacité des étudiants à appliquer leurs connaissances statistiques du cours à de futures opportunités de recherche. En tant qu’instructeurs des cours de statistiques et d’autres cours de psychologie, et forts d’une expérience combinée de plus de 8 ans, nous reconnaissons qu’il existe un décalage entre ce qui se passe dans nos cours et la façon dont les étudiants utilisent (ou N’UTILISENT PAS) les statistiques dans leurs recherches ultérieures.
Mais N’AYEZ PAS PEUR !
C’est là que cette ressource éducative ouverte RS en PNC entre en jeu !
Ici, nous avons travaillé avec un groupe interdisciplinaire d’étudiants diplômés du département de psychologie, de neuroscience et de comportement de l’Université McMaster pour créer un riche ensemble de scénarios de recherche, d’ensembles de données, de plans d’analyse, de questions pratiques et de scripts R qui sont directement liés aux recherches récentes et/ou en cours menées par les membres de la faculté dont vous rejoindrez probablement les laboratoires au cours de l’année ou des deux années à venir ! Ces étudiants diplômés et créateurs de contenu deviennent des experts dans leur domaine en grande partie grâce à une compréhension approfondie des statistiques ainsi qu’à une maîtrise approfondie de R.
Sevda Montakhaby Nodeh et Carmen Tu ont contribué au contenu des chapitres sur les statistiques psychologiques. Dans ces chapitres, vous trouverez des questions sur de nombreux phénomènes psychologiques tels que la perception, l’attention, la cognition, la mémoire, le développement, la narration, la musique et les perceptions sociales. Matin Yousefbadi et Maheshwar Panday ont contribué au contenu des chapitres sur les statistiques liées aux neurosciences. Dans ces chapitres, vous trouverez des questions axées sur la compréhension des électroencéphalogrammes (EEG), de l’imagerie par résonance magnétique (IRM), de l’IRM fonctionnelle (IRMf), ainsi que des aspects clés du traitement des données et de la gestion des ensembles de données à haute dimension. Enfin, Brendan McEwan et Sina Zarini contribuent au contenu des chapitres consacrés à la recherche comportementale, à la recherche sur le comportement animal et aux statistiques. Dans ces chapitres, vous trouverez des questions sur une variété d’espèces animales différentes, y compris les punaises, les mouches, les grenouilles, les lézards et les poissons. Nous n’aurions pas pu trouver une meilleure équipe ni réaliser cette ressource électronique ouverte sans leur dévouement et leurs fantastiques contributions !
Nous espérons que vous pourrez utiliser ce REL pour…
Si vous vous trouvez ici en dehors du département de psychologie, de neuroscience et de comportement de l’université McMaster, vous pouvez toujours bénéficier de la diversité des questions de recherche et des techniques d’analyse présentées ici. L’universalité des statistiques rend ce REL pertinent pour pratiquement tous les contextes dans lesquels vous vous trouvez. Jetez donc un coup d’œil car, après tout, un aspect fondamental de la recherche en psychologie est la connaissance des statistiques.
Avant que vous ne commenciez, nous souhaitons partager quelques remarques sur ce REL. Tout d’abord, il s’agit de la première édition et elle n’est donc pas censée couvrir de manière exhaustive la recherche au sein du PNB. Nous espérons cependant qu’au fil des années, de plus en plus de travaux seront ajoutés afin de rendre compte de l’ensemble des travaux récents et en cours au sein du département. Deuxièmement, vous pouvez participer à ce REL ! Au fur et à mesure que vous terminez vos études, nous vous invitons à soumettre un résumé représentatif de votre recherche, de vos données et de votre analyse. Cela se fait déjà souvent dans le cadre de publications de recherche en libre accès, et il n’y a donc pas grand-chose à faire pour le transformer en ressource éducative. Nous (Ali & Matt) ou quelqu’un de l’équipe, serons plus qu’heureux d’être impliqués dans le processus d’incorporation de votre travail. De cette manière, ce REL sera toujours à jour avec les travaux récents. Troisièmement, explorez ce REL avec un esprit ouvert. Vous constaterez des différences significatives entre les différents domaines de recherche. Vous constaterez que dans différents domaines – et même au sein d’un même domaine – différents chercheurs préfèrent différentes techniques de visualisation. Nous fournissons un échantillon de ce qui peut être fait et espérons qu’il suscitera suffisamment d’intérêt pour que vous puissiez trouver les techniques de visualisation et d’analyse qui répondent le mieux à vos questions.
Alors, amusez-vous bien !
– Ali et Matt
I
En tant que chercheur en sciences cognitives au Cognition and Attention Lab de l’Université McMaster, vous êtes à la pointe de l’exploration des subtilités du contrôle proactif dans les processus d’attention. Cette ligne de recherche est d’une grande importance, étant donné que le système sensoriel humain est submergé par une vaste gamme d’informations à chaque seconde, dépassant ce qui peut être traité de manière significative. L’essence de la recherche sur l’attention consiste à décrypter les mécanismes par lesquels l’entrée sensorielle est parcourue et gérée de manière sélective. Cela est particulièrement important pour comprendre comment les individus anticipent et s’adaptent en vue de tâches ou de stimuli à venir, un phénomène particulièrement pertinent dans des environnements regorgeant de distractions potentielles.
Dans la vie de tous les jours, les conflits attentionnels sont monnaie courante et se manifestent lorsque des informations non pertinentes par rapport à un objectif entrent en compétition avec des données pertinentes par rapport à un objectif pour la priorité attentionnelle. Un exemple de ce phénomène (que nous ne connaissons que trop bien, j’en suis sûr) est la perturbation causée par les notifications sur nos appareils mobiles, qui peuvent nous détourner de nos objectifs principaux, tels que les études ou la conduite. D’un point de vue scientifique, l’élucidation des stratégies employées par le système cognitif humain pour optimiser la sélection et le maintien d’un comportement orienté vers un objectif représente un défi formidable et irrésistible.
Votre recherche en cours est une réponse directe à ce défi. Elle examine comment le contrôle proactif influence la capacité à se concentrer sur les informations pertinentes pour la tâche tout en écartant efficacement les distractions. Cette facette de la fonctionnalité cognitive n’est pas seulement une construction théorique ; c’est le fondement même du comportement et de l’interaction humaine au quotidien.
Votre étude évalue méthodiquement cette dynamique en engageant les participants dans une tâche où ils doivent identifier une séquence de mots dans des conditions variables. Le premier mot (T1) est présenté en rouge, suivi rapidement par un second mot (T2) en blanc. L’intervalle entre l’apparition de T1 et T2, connu sous le nom d’asynchronisme d’apparition du stimulus (SOA), sert de mesure critique dans votre expérience. La particularité de votre étude réside dans la façon dont vous manipulez les demandes d’attention sélective dans chaque essai, classées comme suit :
En introduisant des indices informatifs et non informatifs, votre enquête sonde le rôle du contrôle proactif. Les indices informatifs donnent aux participants un aperçu du type d’épreuve à venir, ce qui leur permet de se préparer mentalement au défi imminent. À l’inverse, les indices non informatifs agissent comme des essais de contrôle et n’offrent aucune indication sur le type d’essai. L’hypothèse est que ces indices informatifs permettent aux participants d’ajuster leur attention de manière proactive en prévision d’un conflit attentionnel, ce qui pourrait améliorer les performances lors des essais de sélection avec des indices informatifs par rapport à ceux avec des indices non informatifs.
Pour une vue d’ensemble des différents types d’essais, veuillez vous référer à la figure ci-dessous. (le texte de la figure demeure toutefois en anglais seulement)
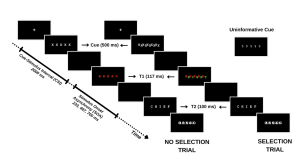
Dans le cadre de cette étude, vous vous attaquez non seulement à la question plus générale du rôle de l’effort conscient dans l’attention, mais vous contribuez également à une compréhension nuancée des processus cognitifs humains, ouvrant la voie à des applications qui vont de l’amélioration de la productivité de la vie quotidienne à l’optimisation des interfaces technologiques en vue d’une perturbation minimale de la cognition.
Commençons par exécuter le code suivant dans RStudio pour charger les bibliothèques requises. Veillez à lire les commentaires intégrés dans le code pour comprendre ce que fait chaque ligne de code.
Remarque : les cases grisées contiennent le code R, le signe “#” indiquant un commentaire qui ne s’exécutera pas dans RStudio.
# Here we create a list called "my_packages" with all of our required libraries
my_packages <- c("tidyverse", "rstatix", "readxl", "xlsx", "emmeans", "afex",
"kableExtra", "grid", "gridExtra", "superb", "ggpubr", "lsmeans")
# Checking and extracting packages that are not already installed
not_installed <- my_packages[!(my_packages %in% installed.packages()[ , "Package"])]
# Install packages that are not already installed
if(length(not_installed)) install.packages(not_installed)
# Loading the required libraries
library(tidyverse) # for data manipulation
library(rstatix) # for statistical analyses
library(readxl) # to read excel files
library(xlsx) # to create excel files
library(kableExtra) # formatting html ANOVA tables
library(superb) # production of summary stat with adjusted error bars(Cousineau, Goulet, & Harding, 2021)
library(ggpubr) # for making plots
library(grid) # for plots
library(gridExtra) # for arranging multiple ggplots for extraction
library(lsmeans) # for pairwise comparisons
Assurez-vous d’avoir téléchargé l’ensemble de données requis (“ProactiveControlCueing.xlsx”) pour cet exercice. Définissez le répertoire de travail de votre session R actuelle dans le dossier contenant l’ensemble de données téléchargé. Vous pouvez le faire manuellement dans le studio R en cliquant sur l’onglet “Session” en haut de l’écran, puis en cliquant sur “Set Working Directory”.
Si le fichier de données téléchargé et votre session R se trouvent dans le même dossier, vous pouvez choisir de définir votre répertoire de travail sur “l’emplacement du fichier source” (l’emplacement où votre session R actuelle est sauvegardée). S’ils se trouvent dans des dossiers différents, cliquez sur l’option “choisir un répertoire” et recherchez l’emplacement du jeu de données téléchargé.
Vous pouvez également effectuer cette opération en exécutant le code suivant
setwd(file.choose())
Une fois que vous avez défini votre répertoire de travail, manuellement ou par code, la console ci-dessous affiche le répertoire complet de votre dossier.
Lisez l’ensemble de données téléchargé sous le nom de “cueingData” et effectuez les exercices qui l’accompagnent au mieux de vos capacités.
# Read xlsx file
cueingData = read_excel("ProactiveControlCueing.xlsx")
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=144#h5p-1
Après avoir configuré les progiciels nécessaires, établi votre répertoire de travail et chargé l’ensemble de données (“cueingData”) dans RStudio, procédez aux exercices ci-dessous. Copiez et collez votre code R dans les zones de texte prévues à cet effet. Vous pouvez exporter les exercices et vos réponses à la fin de cet exercice en tant que fichier docx à partir de la page d’exportation de documents une fois que vous avez terminé.
Une fois les exercices terminés, comparez vos solutions au corrigé inclus ci-dessous. N’oubliez pas que RStudio peut produire des résultats identiques par le biais de différentes méthodes. Ne vous découragez donc pas si votre code diffère du corrigé, à condition que vos résultats soient corrects.
head(cueingData) #Displaying the first few rows## # A tibble: 6 × 6
## ID CUE_TYPE TRIAL_TYPE SOA T1Score T2Score
## <dbl> <chr> <chr> <dbl> <dbl> <dbl>
## 1 1 INFORMATIVE NS 233 100 94.6
## 2 2 INFORMATIVE NS 233 100 97.2
## 3 3 INFORMATIVE NS 233 89.2 93.9
## 4 4 INFORMATIVE NS 233 100 91.9
## 5 5 INFORMATIVE NS 233 100 100
## 6 6 INFORMATIVE NS 233 100 97.3
2. Définissez vos facteurs et vérifiez leur structure. Assurez-vous que vos mesures dépendantes sont sous forme numérique et que vos facteurs et niveaux sont correctement configurés.
cueingData <- cueingData %>%
convert_as_factor(ID, CUE_TYPE, TRIAL_TYPE, SOA) #setting up factors
str(cueingData) #checking that factors and levels are set-up correctly. Checking to see that dependent measures are in numerical format.
## # A tibble: 6 × 6
## ID CUE_TYPE TRIAL_TYPE SOA T1Score T2Score
## <dbl> <chr> <chr> <dbl> <dbl> <dbl>
## 1 1 INFORMATIVE NS 233 100 94.6
## 2 2 INFORMATIVE NS 233 100 97.2
## 3 3 INFORMATIVE NS 233 89.2 93.9
## 4 4 INFORMATIVE NS 233 100 91.9
## 5 5 INFORMATIVE NS 233 100 100
## 6 6 INFORMATIVE NS 233 100 97.3
## tibble [192 × 6] (S3: tbl_df/tbl/data.frame)
## $ ID : Factor w/ 16 levels "1","2","3","4",..: 1 2 3 4 5 6 7 8 9 10 ...
## $ CUE_TYPE : Factor w/ 2 levels "INFORMATIVE",..: 1 1 1 1 1 1 1 1 1 1 ...
## $ TRIAL_TYPE: Factor w/ 2 levels "NS","S": 1 1 1 1 1 1 1 1 1 1 ...
## $ SOA : Factor w/ 3 levels "233","467","700": 1 1 1 1 1 1 1 1 1 1 ...
## $ T1Score : num [1:192] 100 100 89.2 100 100 ...
## $ T2Score : num [1:192] 94.6 97.2 93.9 91.9 100 ...
3. Effectuer des contrôles de base des données pour vérifier les valeurs manquantes et la cohérence des données
sum(is.na(cueingData)) # Checking for missing values in the dataset
## [1] 0
summary(cueingData) # Viewing the summary of the dataset to check for inconsistencies
## ID CUE_TYPE TRIAL_TYPE SOA T1Score
## 1 : 12 INFORMATIVE :96 NS:96 233:64 Min. : 32.43
## 2 : 12 UNINFORMATIVE:96 S :96 467:64 1st Qu.: 77.78
## 3 : 12 700:64 Median : 95.87
## 4 : 12 Mean : 86.33
## 5 : 12 3rd Qu.:100.00
## 6 : 12 Max. :100.00
## (Other):120
## T2Score
## Min. : 29.63
## 1st Qu.: 83.97
## Median : 95.76
## Mean : 87.84
## 3rd Qu.:100.00
## Max. :100.00
table(cueingData$CUE_TYPE, cueingData$TRIAL_TYPE, cueingData$SOA) #checking the number of observations per condition or combination of factors. Data is a balanced design since there is an equal number of observations per cell.## , , = 233
##
##
## NS S
## INFORMATIVE 16 16
## UNINFORMATIVE 16 16
##
## , , = 467
##
##
## NS S
## INFORMATIVE 16 16
## UNINFORMATIVE 16 16
##
## , , = 700
##
##
## NS S
## INFORMATIVE 16 16
## UNINFORMATIVE 16 16
Nous utiliserons ici la bibliothèque Superb pour calculer nos statistiques sommaires avec l’erreur standard des mesures moyennes qui ont été corrigées pour les comparaisons entre sujets.
Pour vous familiariser avec la bibliothèque Superb, je vous suggère de lire l’article publié suivant et de regarder les tutoriels YouTube.
Cousineau D, Goulet M, Harding B (2021). “Graphiques sommaires avec barres d’erreur ajustées : The superb framework with an implementation in R.” Advances in Methods and Practices in Psychological Science, 2021, 1-46. doi : https://doi.org/10.1177/25152459211035109
Walker, J. A. L. (2021). “Summary plots with adjusted error bars (superb)”. Vidéo Youtube, accessible ici.
Walker, J. A. L. (2021). Summary plots with adjusted error bars (superb). Extrait de https://www.youtube.com/watch?v=rw_6ll5nVus
Pour jouer avec les différentes fonctionnalités de la bibliothèque superb, une application Shiny avec une vue de constructeur pour la bibliothèque est également disponible sur le web. Vous trouverez également ci-dessous une ressource utile pour naviguer dans le code R de la bibliothèque Superb.
5. La bibliothèque Superb exige que votre jeu de données soit dans un format large. Convertissez donc votre jeu de données d’un format long à un format large. Enregistrez-le sous “cueingData.wide”.
cueingData.wide <- cueingData %>%
pivot_wider(names_from = c(TRIAL_TYPE, SOA, CUE_TYPE),
values_from = c(T1Score, T2Score) )
6. En utilisant superbPlot() et cueingData.wide, calculez la moyenne et l’erreur standard de la moyenne (SEM) pour les scores T1 et T2 à chaque niveau des facteurs. Veillez à calculer les valeurs SEM corrigées de Cousineau-Morey.
EXP1.T1.plot <- superbPlot(cueingData.wide,
WSFactors = c("SOA(3)", "CueType(2)", "TrialType(2)"),
variables = c("T1Score_NS_233_INFORMATIVE", "T1Score_NS_467_INFORMATIVE",
"T1Score_NS_700_INFORMATIVE", "T1Score_NS_233_UNINFORMATIVE",
"T1Score_NS_467_UNINFORMATIVE", "T1Score_NS_700_UNINFORMATIVE",
"T1Score_S_233_INFORMATIVE", "T1Score_S_467_INFORMATIVE",
"T1Score_S_700_INFORMATIVE", "T1Score_S_233_UNINFORMATIVE",
"T1Score_S_467_UNINFORMATIVE", "T1Score_S_700_UNINFORMATIVE"),
statistic = "mean",
errorbar = "SE",
adjustments = list(
purpose = "difference",
decorrelation = "CM",
popSize = 32
),
plotStyle = "line",
factorOrder = c("SOA", "CueType", "TrialType"),
lineParams = list(size=1, linetype="dashed"),
pointParams = list(size = 3))
## superb::FYI: Here is how the within-subject variables are understood:
## SOA CueType TrialType variable
## 1 1 1 T1Score_NS_233_INFORMATIVE
## 2 1 1 T1Score_NS_467_INFORMATIVE
## 3 1 1 T1Score_NS_700_INFORMATIVE
## 1 2 1 T1Score_NS_233_UNINFORMATIVE
## 2 2 1 T1Score_NS_467_UNINFORMATIVE
## 3 2 1 T1Score_NS_700_UNINFORMATIVE
## 1 1 2 T1Score_S_233_INFORMATIVE
## 2 1 2 T1Score_S_467_INFORMATIVE
## 3 1 2 T1Score_S_700_INFORMATIVE
## 1 2 2 T1Score_S_233_UNINFORMATIVE
## 2 2 2 T1Score_S_467_UNINFORMATIVE
## 3 2 2 T1Score_S_700_UNINFORMATIVE
## superb::FYI: The HyunhFeldtEpsilon measure of sphericity per group are 0.134
## superb::FYI: Some of the groups' data are not spherical. Use error bars with caution.
EXP1.T2.plot <- superbPlot(cueingData.wide,
WSFactors = c("SOA(3)", "CueType(2)", "TrialType(2)"),
variables = c("T2Score_NS_233_INFORMATIVE", "T2Score_NS_467_INFORMATIVE",
"T2Score_NS_700_INFORMATIVE", "T2Score_NS_233_UNINFORMATIVE",
"T2Score_NS_467_UNINFORMATIVE", "T2Score_NS_700_UNINFORMATIVE",
"T2Score_S_233_INFORMATIVE", "T2Score_S_467_INFORMATIVE",
"T2Score_S_700_INFORMATIVE", "T2Score_S_233_UNINFORMATIVE",
"T2Score_S_467_UNINFORMATIVE", "T2Score_S_700_UNINFORMATIVE"),
statistic = "mean",
errorbar = "SE",
adjustments = list(
purpose = "difference",
decorrelation = "CM",
popSize = 32
),
plotStyle = "line",
factorOrder = c("SOA", "CueType", "TrialType"),
lineParams = list(size=1, linetype="dashed"),
pointParams = list(size = 3)
)
## superb::FYI: Here is how the within-subject variables are understood:
## SOA CueType TrialType variable
## 1 1 1 T2Score_NS_233_INFORMATIVE
## 2 1 1 T2Score_NS_467_INFORMATIVE
## 3 1 1 T2Score_NS_700_INFORMATIVE
## 1 2 1 T2Score_NS_233_UNINFORMATIVE
## 2 2 1 T2Score_NS_467_UNINFORMATIVE
## 3 2 1 T2Score_NS_700_UNINFORMATIVE
## 1 1 2 T2Score_S_233_INFORMATIVE
## 2 1 2 T2Score_S_467_INFORMATIVE
## 3 1 2 T2Score_S_700_INFORMATIVE
## 1 2 2 T2Score_S_233_UNINFORMATIVE
## 2 2 2 T2Score_S_467_UNINFORMATIVE
## 3 2 2 T2Score_S_700_UNINFORMATIVE
## superb::FYI: The HyunhFeldtEpsilon measure of sphericity per group are 0.226
## superb::FYI: Some of the groups' data are not spherical. Use error bars with caution.
# Re-naming levels of the factors
levels(EXP1.T1.plot$data$SOA) <- c("1" = "233", "2" = "467", "3" = "700")
levels(EXP1.T2.plot$data$SOA) <- c("1" = "233", "2" = "467", "3" = "700")
levels(EXP1.T1.plot$data$TrialType) <- c("1" = "No Selection", "2" = "Selection")
levels(EXP1.T2.plot$data$TrialType) <- c("1" = "No Selection", "2" = "Selection")
levels(EXP1.T1.plot$data$CueType) <- c("1" = "Informative", "2" = "Uninformative")
levels(EXP1.T2.plot$data$CueType) <- c("1" = "Informative", "2" = "Uninformative")
7. Créons un magnifique tableau HTML imprimable des statistiques récapitulatives pour les scores T1 et T2. Ce tableau récapitulatif peut ensuite être utilisé dans votre manuscrit. Je vous suggère de visiter le lien suivant pour obtenir des guides sur la façon de créer des tableaux imprimables. Personnalisation du tableau HTML
# Extracting summary data with CousineauMorey SEM Bars
EXP1.T1.summaryData <- data.frame(EXP1.T1.plot$data)
EXP1.T2.summaryData <- data.frame(EXP1.T2.plot$data)
# Rounding values in each column
# round(x, 1) rounds to the specified number of decimal places
EXP1.T1.summaryData$center <- round(EXP1.T1.summaryData$center,1)
EXP1.T1.summaryData$upperwidth <- round(EXP1.T1.summaryData$upperwidth,2)
EXP1.T2.summaryData$center <- round(EXP1.T2.summaryData$center,1)
EXP1.T2.summaryData$upperwidth <- round(EXP1.T2.summaryData$upperwidth,2)
# merging T1 and T2|T1 summary tables
EXP1_summarystat_results <- merge(EXP1.T1.summaryData, EXP1.T2.summaryData, by=c("TrialType","CueType","SOA"))
# Rename the column name
colnames(EXP1_summarystat_results)[colnames(EXP1_summarystat_results) == "center.x"] ="Mean"
colnames(EXP1_summarystat_results)[colnames(EXP1_summarystat_results) == "center.y"] ="Mean"
colnames(EXP1_summarystat_results)[colnames(EXP1_summarystat_results) == "upperwidth.x"] ="SEM"
colnames(EXP1_summarystat_results)[colnames(EXP1_summarystat_results) == "upperwidth.y"] ="SEM"
# deleting columns by name "lowerwidth.x" and "lowerwidth.y" in each summary table
EXP1_summarystat_results <- EXP1_summarystat_results[ , ! names(EXP1_summarystat_results) %in% c("lowerwidth.x", "lowerwidth.y")]
#removing suffixes from column names
colnames(EXP1_summarystat_results)<-gsub(".1","",colnames(EXP1_summarystat_results))
# Printable ANOVA html
EXP1_summarystat_results %>%
kbl(caption = "Summary Statistics") %>%
kable_classic(full_width = F, html_font = "Cambria", font_size = 14) %>%
add_header_above(c(" " = 3, "T1 Accuracy (%)" = 2, "T2|T1 Accuracy (%)" = 2))
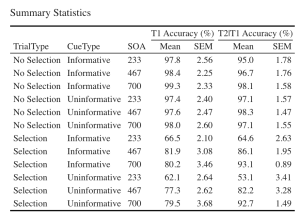
8. Utilisez le tableau de statistiques récapitulatives non édité de l’exercice 2 (EXP1.T1.summaryData et EXP1.T3.summaryData) et la fonction ggplot() pour créer des graphiques linéaires récapitulatifs distincts pour les scores T1 et T2. Le graphique linéaire visualise la relation entre la SOA et la mesure dépendante tout en tenant compte des facteurs de type de repère et de type d’essai. Votre graphique doit présenter les caractéristiques suivantes :
EXP1.T1.ggplotplot <- ggplot(EXP1.T1.summaryData, aes(x=SOA, y=center, color=TrialType, shape = CueType,
group=interaction(CueType, TrialType))) +
geom_point(data=filter(EXP1.T1.summaryData, CueType == "Uninformative"), shape=1, size=4.5) + # assigning shape type to level of factor
geom_point(data=filter(EXP1.T1.summaryData, CueType == "Informative"), shape=16, size=4.5) + # assigning shape type to level of factor
geom_line(linetype="dashed", linewidth=1.2) + # change line thickness and line style
scale_color_manual(values = c("gray78", "black") ) +
xlab("SOA (ms)") +
ylab("T1 Identification Accuracy (%)") +
theme_classic() + # It has no background, no bounding box.
theme(axis.line=element_line(size=1.5), # We make the axes thicker...
axis.text = element_text(size = 14, colour = "black"), # their text bigger...
axis.title = element_text(size = 16, colour = "black"), # their labels bigger...
panel.grid.major.y = element_line(), # adding horizontal grid lines
legend.position = "none") +
coord_cartesian(ylim=c(30, 100)) +
scale_y_continuous(breaks=seq(30, 100, 10)) + # Ticks from 30-100, every 10
geom_errorbar(aes(ymin=center+lowerwidth, ymax=center+upperwidth), width = 0.12, size = 1) # adding error bars from summary table
EXP1.T2.ggplotplot <- ggplot(EXP1.T2.summaryData, aes(x=SOA, y=center, color=TrialType, shape=CueType,
group=interaction(CueType, TrialType))) +
geom_point(data=filter(EXP1.T2.summaryData, CueType == "Uninformative"), shape=1, size=4.5) + # assigning shape type to level of factor
geom_point(data=filter(EXP1.T2.summaryData, CueType == "Informative"), shape=16, size=4.5) + # assigning shape type to level of factor
geom_line(linetype="dashed", linewidth=1.2) + # change line thickness and line style
scale_color_manual(values = c("gray78", "black")) +
xlab("SOA (ms)") +
ylab("T2|T1 Identification Accuracy (%)") +
theme_classic() + # It has no background, no bounding box.
theme(axis.line=element_line(size=1.5), # We make the axes thicker...
axis.text = element_text(size = 14, colour = "black"), # their text bigger...
axis.title = element_text(size = 16, colour = "black"), # their labels bigger...
panel.grid.major.y = element_line(), # adding horizontal grid lines
legend.position = "none") +
guides(fill = guide_legend(override.aes = list(shape = 16) ),
shape = guide_legend(override.aes = list(fill = "black"))) +
coord_cartesian(ylim=c(30, 100)) +
scale_y_continuous(breaks=seq(30, 100, 10)) + # Ticks from 30-100, every 10
geom_errorbar(aes(ymin=center+lowerwidth, ymax=center+upperwidth), width = 0.12, size = 1) # adding error bars from summary table
9. Utilisez ggarrange() pour afficher vos tracés ensemble.
ggarrange(EXP1.T1.ggplotplot, EXP1.T2.ggplotplot,
nrow = 1, ncol = 2, common.legend = F,
widths = 8, heights = 5)
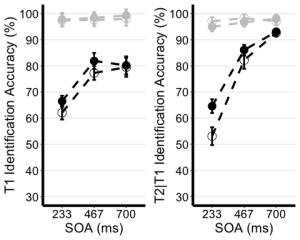
Étant donné que les performances des essais de non-sélection sont proches du plafond (près de 100 %), nous concentrerons nos analyses sur les essais de sélection.
10. Utilisez les données en format long (“cueingData”) et la fonction anova_test(), et calculez une ANOVA à deux voies pour chaque variable dépendante, mais sur les essais de sélection uniquement. Définissez le type de repère et l’AOS comme facteurs internes aux participants. (Conseil : utilisez la fonction filter())
T1_2anova <- anova_test(
data = filter(cueingData, TRIAL_TYPE == "S"), dv = T1Score, wid = ID,
within = c(CUE_TYPE, SOA), detailed = TRUE, effect.size = "pes")
T2_2anova <- anova_test(
data = filter(cueingData, TRIAL_TYPE == "S"), dv = T2Score, wid = ID,
within = c(CUE_TYPE, SOA), detailed = TRUE, effect.size = "pes")
get_anova_table(T1_2anova)
## ANOVA Table (type III tests)
##
## Effect DFn DFd SSn SSd F p p<.05 pes
## 1 (Intercept) 1.00 15.00 534043.211 30705.523 260.886 6.80e-11 * 0.946
## 2 CUE_TYPE 1.00 15.00 253.665 506.454 7.513 1.50e-02 * 0.334
## 3 SOA 1.29 19.35 5091.853 2660.275 28.710 1.16e-05 * 0.657
## 4 CUE_TYPE:SOA 2.00 30.00 77.140 1061.051 1.091 3.49e-01 0.068
get_anova_table(T2_2anova)
## ANOVA Table (type III tests)
##
## Effect DFn DFd SSn SSd F p p<.05 pes
## 1 (Intercept) 1 15 593913.106 11288.706 789.169 2.19e-14 * 0.981
## 2 CUE_TYPE 1 15 661.761 426.947 23.250 2.24e-04 * 0.608
## 3 SOA 2 30 20001.563 3852.629 77.875 1.33e-12 * 0.838
## 4 CUE_TYPE:SOA 2 30 519.154 1298.144 5.999 6.00e-03 * 0.286
S’il existe une interaction bidirectionnelle significative, cela signifie que l’impact d’un facteur est influencé par un autre facteur. Cela signifie que les deux variables indépendantes interagissent l’une avec l’autre pour produire un effet significatif sur la variable dépendante. Étant donné qu’il existe une interaction bidirectionnelle significative entre le type de repère et l’AOS pour les scores T2, nous devons procéder à des tests post hoc afin d’explorer et de comprendre les différences spécifiques entre les niveaux ou les conditions des facteurs impliqués dans l’interaction. Cela peut nous aider à identifier les combinaisons spécifiques à l’origine de l’effet d’interaction.
11. Filtrez d’abord les essais de sélection, puis regroupez vos données par SOA et utilisez la fonction pairwise_t_test() pour comparer les essais informatifs et non informatifs à chaque niveau de SOA, stockez et affichez votre calcul sous la forme “T2_sel_pwc”.
T2_sel_pwc <- filter(cueingData, TRIAL_TYPE == "S") %>%
group_by(SOA) %>%
pairwise_t_test(T2Score ~ CUE_TYPE, paired = TRUE, p.adjust.method = "holm", detailed = TRUE) %>%
add_significance("p.adj")
T2_sel_pwc <- get_anova_table(T2_sel_pwc)
T2_sel_pwc
## # A tibble: 3 × 16
## SOA estimate .y. group1 group2 n1 n2 statistic p df
## <fct> <dbl> <chr> <chr> <chr> <int> <int> <dbl> <dbl> <dbl>
## 1 233 11.5 T2Score INFORMATIVE UNINFO… 16 16 4.36 5.55e-4 15
## 2 467 3.89 T2Score INFORMATIVE UNINFO… 16 16 1.97 6.8 e-2 15
## 3 700 0.356 T2Score INFORMATIVE UNINFO… 16 16 0.190 8.52e-1 15
## # ℹ 6 more variables: conf.low <dbl>, conf.high <dbl>, method <chr>,
## # alternative <chr>, p.adj <dbl>, p.adj.signif <chr>
Superbe travail !
Vous avez réussi à reconstruire une figure et à effectuer des analyses dans le cadre d’un projet de mémoire de maîtrise. Les données sur lesquelles vous avez travaillé ont été recueillies dans le laboratoire d’attention et de mémoire du département de psychologie, de neuroscience et de comportement (PNB) de l’Université McMaster. Ce laboratoire prospère sous l’égide du Dr Bruce Milliken, dont les recherches sont profondément ancrées dans le domaine de la cognition humaine. L’objectif principal du laboratoire est d’élucider les processus fondamentaux qui sous-tendent l’attention, la mémoire et le contrôle cognitif. L’étendue des recherches menées ici englobe un large éventail de sujets. Il s’agit notamment d’étudier les nuances qui différencient les processus mentaux conscients et inconscients, d’explorer la manière dont les mécanismes attentionnels influencent et soutiennent l’apprentissage et la mémoire, de comprendre le rôle de l’imagerie visuelle dans la formation de l’attention et de la perception, et d’examiner l’impact de l’apprentissage implicite sur l’orchestration du contrôle de l’attention. Chaque projet au sein de ce laboratoire témoigne de l’engagement à faire progresser notre compréhension de la tapisserie complexe de la cognition humaine.
Si vous souhaitez approfondir l’ensemble des données et les spécificités du projet de thèse, je vous encourage à explorer la thèse de doctorat librement accessible ou l’article publié cité ci-dessous :
Montakhaby Nodeh, S., MacLellan, E., & Milliken, B. (2024). Proactive control: Endogenous cueing effects in a two-target attentional blink task. Consciousness and Cognition, 118, 103648. Elsevier BV. https://doi.org/10.1016/j.concog.2024.103648
Bienvenue ! Dans le cadre de cette tâche, nous allons entrer dans un laboratoire de cognition et de mémoire de l’Université McMaster. Plus précisément, nous examinerons les données d’une étude fascinante de psychologie cognitive qui explore le rôle de la répétition dans la mémoire de reconnaissance.
La plupart d’entre nous connaissent l’expression “c’est en forgeant qu’on devient forgeron”. Cette expression motivante correspond à l’intuition et est confirmée par de nombreuses observations dans le monde réel. De nombreuses recherches empiriques soutiennent également ce point de vue : les occasions répétées d’encoder un stimulus améliorent la récupération ultérieure de la mémoire et l’identification perceptuelle. Ces observations suggèrent que la répétition d’un stimulus renforce les représentations sous-jacentes dans la mémoire.
La présente étude se concentre sur une idée contradictoire, à savoir que la répétition d’un stimulus peut affaiblir l’encodage de la mémoire. L’expérience comprenait trois étapes : une phase d’étude, une phase de distraction et un test de mémoire de reconnaissance surprise.
La présente étude se concentre sur une idée contradictoire, à savoir que la répétition du stimulus peut affaiblir l’encodage de la mémoire. L’expérience comprenait trois étapes : une phase d’étude, une phase de distraction et un test de mémoire de reconnaissance par surprise.
Dans la phase d’étude, les participants prononcent à haute voix un mot cible rouge précédé d’un mot premier vert brièvement présenté. Sur la moitié des essais, le mot principal et le mot cible étaient identiques (essais répétés), et sur l’autre moitié des essais, le mot principal et le mot cible étaient différents (essais non répétés). La figure ci-dessous donne un aperçu des deux types d’essais. Après la phase d’étude, les participants se sont livrés à une tâche de distraction de 10 minutes consistant en des problèmes mathématiques qu’ils devaient résoudre à la main.
La phase finale consistait en un test de mémoire de reconnaissance surprise où, à chaque essai, on leur montrait un mot rouge et on leur demandait de répondre “ancien” si le mot du test était un mot qu’ils avaient déjà vu à l’étude, et “nouveau” s’ils n’avaient jamais rencontré ce mot auparavant. La moitié des essais du test étaient des mots de la phase d’étude et l’autre moitié des mots nouveaux.
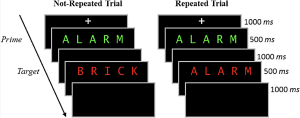
Commençons par exécuter le code suivant pour charger les bibliothèques requises. Veillez à lire les commentaires intégrés dans le code pour comprendre ce que fait chaque ligne de code.
# Load necessary libraries
library(rstatix) #for performing basic statistical tests
library(dplyr) #for sorting data
library(readxl) #for reading excel files
library(tidyr) #for data sorting and structure
library(ggplot2) #for visualizing your data
library(plotrix) #for computing basic summary stats
Assurez-vous d’avoir téléchargé l’ensemble de données requis (“RepDecrementdataset.xlsx”) pour cet exercice. Définissez le répertoire de travail de votre session R actuelle dans le dossier contenant l’ensemble de données téléchargé. Vous pouvez le faire manuellement dans le studio R en cliquant sur l’onglet “Session” en haut de l’écran, puis en cliquant sur “Set Working Directory”.
Si le fichier de données téléchargé et votre session R se trouvent dans le même dossier, vous pouvez choisir de définir votre répertoire de travail sur “l’emplacement du fichier source” (l’emplacement où votre session R actuelle est sauvegardée). S’ils se trouvent dans des dossiers différents, cliquez sur l’option “choisir un répertoire” et recherchez l’emplacement du jeu de données téléchargé.
Vous pouvez également effectuer cette opération en exécutant le code suivant
setwd(file.choose())
Une fois que vous avez défini votre répertoire de travail, manuellement ou par code, la console ci-dessous affiche le répertoire complet de votre dossier.
Lisez l’ensemble de données téléchargé en tant que “MemoryData” et effectuez les exercices qui l’accompagnent au mieux de vos capacités.
MemoryData <- read_excel('RepDecrementdataset.xlsx')
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=148#h5p-2
1. Affichez les premières lignes de votre jeu de données pour vous familiariser avec sa structure et son contenu.
head(MemoryData) #Displaying the first few rows
## # A tibble: 6 × 7
## ID Hits_NRep Hits_Rep FalseAlarms Misses_Nrep Misses_Rep CorrectRej
## <dbl> <dbl> <dbl> <dbl> <dbl> <dbl> <dbl>
## 1 1 46 34 13 14 26 107
## 2 2 43 44 27 17 16 93
## 3 3 43 35 23 17 24 97
## 4 4 37 36 56 23 24 64
## 5 5 39 35 49 21 25 71
## 6 6 38 43 28 22 17 92
str(MemoryData) #Checking structure of dataset
## tibble [24 × 7] (S3: tbl_df/tbl/data.frame)
## $ ID : num [1:24] 1 2 3 4 5 6 7 8 9 10 ...
## $ Hits_NRep : num [1:24] 46 43 43 37 39 38 20 24 36 38 ...
## $ Hits_Rep : num [1:24] 34 44 35 36 35 43 11 29 43 27 ...
## $ FalseAlarms: num [1:24] 13 27 23 56 49 28 4 11 46 9 ...
## $ Misses_Nrep: num [1:24] 14 17 17 23 21 22 40 36 23 22 ...
## $ Misses_Rep : num [1:24] 26 16 24 24 25 17 49 31 17 33 ...
## $ CorrectRej : num [1:24] 107 93 97 64 71 92 116 109 74 111 ...
colnames(MemoryData)
## [1] "ID" "Hits_NRep" "Hits_Rep" "FalseAlarms" "Misses_Nrep"
## [6] "Misses_Rep" "CorrectRej"
2. Calculer le nombre total d’essais pour chaque condition :
Notez que si la valeur de “TotalNRep” et “TotalRep” est inférieure à 60 pour un participant, cela indique que certains essais de mots ont été exclus pendant la phase d’étude en raison de problèmes (par exemple, le participant a lu à haute voix le mot principal au lieu du mot cible, ce qui a entraîné la détérioration de l’essai).
MemoryData <- MemoryData %>%
mutate(TotalNRep = Hits_NRep + Misses_Nrep)
MemoryData <- MemoryData %>%
mutate(TotalRep = Hits_Rep + Misses_Rep)
MemoryData <- MemoryData %>%
mutate(TotalNew = FalseAlarms + CorrectRej)
3. Transformez les nombres des colonnes “hits”, “misses”, “false alarms” et “correct rejections” en proportions. Pour ce faire, divisez chaque nombre par le nombre total d’essais pour la condition concernée (par exemple, divisez les réponses positives pour les essais non répétés par “TotalNRep”).
MemoryData$Hits_NRep <- (MemoryData$Hits_NRep/MemoryData$TotalNRep)
MemoryData$Misses_Nrep <- (MemoryData$Misses_Nrep/MemoryData$TotalNRep)
MemoryData$Hits_Rep <- (MemoryData$Hits_Rep/MemoryData$TotalRep)
MemoryData$Misses_Rep <- (MemoryData$Misses_Rep/MemoryData$TotalRep)
MemoryData$CorrectRej <- (MemoryData$CorrectRej/MemoryData$TotalNew)
MemoryData$FalseAlarms <- (MemoryData$FalseAlarms/MemoryData$TotalNew)
4. Une fois les proportions calculées, supprimez les colonnes “TotalNew”, “TotalRep” et “TotalNRep” de l’ensemble de données, car elles ne sont plus nécessaires pour la suite de l’analyse.
MemoryData <- MemoryData[, !names(MemoryData) %in% c("TotalNew", "TotalRep","TotalNRep")]
5. Utilisez la fonction pivot_longer() du package tidyr pour convertir vos données du format large au format long. Effectuez un pivot des colonnes “Hits_NRep”, “Hits_Rep” et “FalseAlarms”, en définissant les nouveaux noms de colonnes “Condition” et “Proportion” pour les données remodelées.
long_df <- MemoryData %>%
pivot_longer(
cols = c(Hits_NRep, Hits_Rep, FalseAlarms),
names_to = "Condition",
values_to = "Proportion"
)
6. À l’aide de votre ensemble de données au format long, regroupez vos données par ID et calculez la moyenne par sujet et la moyenne générale de la colonne Proportions.
data_adjusted <- long_df %>%
group_by(ID) %>%
mutate(SubjectMean = mean(Proportion, na.rm = TRUE)) %>%
ungroup() %>%
mutate(GrandMean = mean(Proportion, na.rm = TRUE)) %>%
mutate(AdjustedScore = Proportion - SubjectMean + GrandMean)
# Calculate the mean and SEM of the adjusted scores
summary_df <- data_adjusted %>%
group_by(Condition) %>%
summarize(
AdjustedMean = mean(AdjustedScore, na.rm = TRUE),
AdjustedSEM = sd(AdjustedScore, na.rm = TRUE) / sqrt(n())
)
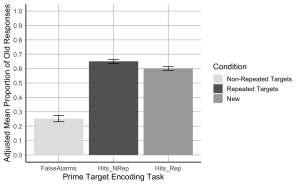
7. Créez un diagramme à barres où l’axe x représente les conditions de la tâche d’encodage de l’amorce et de la cible, l’axe y montre la proportion moyenne ajustée des anciennes réponses, et les barres d’erreur représentent le SEM ajusté. Commencez par définir des couleurs personnalisées pour chaque condition. La couleur de la barre présentant les fausses alarmes ou “New” doit être “gray89” ; la couleur de la barre “Hits_Nrep” ou “Non-Repeated Targets” doit être “gray39” ; la couleur de la barre “Hits_Rep” ou “Repeated Targets” doit être “darkgrey”.
# Create the bar plot with adjusted SEM error bars
ggplot(summary_df, aes(x = Condition, y = AdjustedMean, fill = Condition)) +
geom_bar(stat = "identity", position = position_dodge()) +
geom_errorbar(aes(ymin = AdjustedMean - AdjustedSEM, ymax = AdjustedMean + AdjustedSEM), width = 0.2, position = position_dodge(0.9)) +
scale_fill_manual(values = c("Hits_NRep" = "gray39", "Hits_Rep" = "darkgrey", "FalseAlarms" = "gray89"),
labels = c("Non-Repeated Targets", "Repeated Targets", "New")) +
labs(
x = "Prime Target Encoding Task",
y = "Adjusted Mean Proportion of Old Responses",
fill = "Condition"
) +
scale_y_continuous(breaks = seq(0, 1, by = 0.1), limits = c(0, 1)) +
theme_minimal(base_size = 14) +
theme(
axis.line = element_line(color = "black"),
axis.title = element_text(color = "black"),
panel.grid.major = element_line(color = "grey", size = 0.5),
panel.grid.minor = element_blank(),
legend.title = element_text(color = "black")
)
8. À l’aide du fichier de données au format large “MemoryData”, effectuez un test t à deux échantillons appariés en comparant le taux de réussite cumulé dans les deux conditions de répétition (répété/non répété) au taux de fausses alarmes pour évaluer la capacité des participants à distinguer les anciens éléments des nouveaux.
collapsed_hitdata <- MemoryData %>%
mutate(HitRate = (Hits_NRep + Hits_Rep) / 2)
# Conduct paired sample t-tests
t_test_results <- t.test(collapsed_hitdata$HitRate, collapsed_hitdata$FalseAlarms, paired = TRUE)
print(t_test_results)
##
## Paired t-test
##
## data: collapsed_hitdata$HitRate and collapsed_hitdata$FalseAlarms
## t = 11.621, df = 23, p-value = 4.179e-11
## alternative hypothesis: true mean difference is not equal to 0
## 95 percent confidence interval:
## 0.3071651 0.4401983
## sample estimates:
## mean difference
## 0.3736817
#Hit rates were higher than false alarm rates, t(23) = 11.62, p < .001.
9. En utilisant le fichier de données au format large “MemoryData”, effectuez un test t à deux échantillons appariés comparant les taux de réussite pour les cibles non répétées et répétées.
# Conduct paired sample t-tests for non-repeated vs repeated hit rates
t_test_results_hits <- t.test(collapsed_hitdata$Hits_NRep, collapsed_hitdata$Hits_Rep, paired = TRUE)
# Print the results for the hit rate comparison
print(t_test_results_hits)
##
## Paired t-test
##
## data: collapsed_hitdata$Hits_NRep and collapsed_hitdata$Hits_Rep
## t = 2.5431, df = 23, p-value = 0.01817
## alternative hypothesis: true mean difference is not equal to 0
## 95 percent confidence interval:
## 0.009071364 0.088174399
## sample estimates:
## mean difference
## 0.04862288
#Hit rates were higher for not-repeated targets than for repeated targets, t(23) = 2.54, p = .018.
Vous êtes chercheur au Centre de recherche sur le développement de la petite enfance. Votre dernier projet porte sur la manière dont les nourrissons réagissent à différentes combinaisons de visages, de races et d’émotions musicales. Plus précisément, vous vous intéressez à la question de savoir si les enfants associent des visages de leur propre race et d’autres races à des musiques de différentes valences émotionnelles (musique joyeuse et musique triste).
Votre projet a été réalisé en collaboration avec vos collègues en Chine. Alors que vous étiez responsable de la conception de votre expérience, vos collaborateurs étaient chargés de recruter les participants et de collecter les données.
Des bébés chinois (âgés de 3 à 9 mois) ont été recrutés pour participer à votre expérience. Chaque enfant a été assigné au hasard à l’une des quatre conditions visage-race + musique dans lesquelles il voyait une série de visages neutres de sa propre race ou d’une autre race associés à des extraits musicaux joyeux ou tristes.
Dans le cadre de l’expérience “own-happy”, les enfants ont regardé six vidéos de visages asiatiques associées de manière séquentielle à six extraits musicaux joyeux. Dans l’autre condition, les enfants ont regardé six vidéos de visages africains associés séquentiellement à des extraits musicaux joyeux. En général, les conditions étaient identiques sur le plan procédural, à l’exception de la composition du visage et de la musique. Les mouvements oculaires des enfants ont été enregistrés à l’aide d’un système de suivi des yeux.
Votre objectif est de déterminer comment la race du visage et l’émotion de la musique, ainsi que leur interaction, influencent le comportement des nourrissons en matière de regard.
Vos variables indépendantes :
Vos variables dépendantes :
Commençons par charger les bibliothèques nécessaires et le jeu de données “BabyData”. Pour ce faire, téléchargez le fichier “infant_eye_tracking_study.csv” et exécutez le code suivant. N’oubliez pas de remplacer ‘path_to_your_downloaded_file’ par le chemin réel du jeu de données sur votre système.
BabyData <- read.csv('path_to_your_downloaded_file/infant_eye_tracking_study.csv')
library(rstatix) #for performing basic statistical tests
library(dplyr) #for sorting data
library(tidyr) #for data sorting and structure
library(ggplot2) #for visualizing your data
library(readr)
library(ggpubr)
library(gridExtra)
Veuillez compléter les exercices ci-joints au mieux de vos capacités.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=152#h5p-3
1. Affichez les premières lignes pour comprendre votre jeu de données.
summary(BabyData) # Viewing the summary of the dataset to check for inconsistencies
## Age.in.Days Condition Face.Race Music.Emotion Age.Group
## 1 93 Other-Race Happy Music African happy 3
## 2 98 Other-Race Happy Music African happy 3
## 3 93 Other-Race Happy Music African happy 3
## 4 93 Other-Race Happy Music African happy 3
## 5 93 Other-Race Happy Music African happy 3
## 6 100 Other-Race Happy Music African happy 3
## Total.Looking.Time First.Face.Looking.Time Participant.ID
## 1 44.035 8.273 HJOGM7704U
## 2 18.324 6.938 JHSEG5414N
## 3 24.600 4.225 OCQFX4970K
## 4 12.919 7.537 KLDOF5559R
## 5 12.755 4.230 HHPGJ9661Y
## 6 38.777 9.351 NVCPX9518V
2. Utilisez relocate() pour réorganiser vos colonnes de manière à ce que la colonne “Participant.ID” apparaisse comme la première colonne de votre ensemble de données.
BabyData <- BabyData %>% relocate(Participant.ID, .before = Age.in.Days)
3. Vérifiez que vos données ne comportent pas de valeurs manquantes. Supprimez de l’ensemble de données toutes les lignes contenant des valeurs manquantes ou NA.
sum(is.na(BabyData)) # Checking for missing values in the dataset
## [1] 3
BabyData <- BabyData[!is.na(BabyData$First.Face.Looking.Time), ]
## Participant.ID Age.in.Days Condition Face.Race
## Length:193 Min. : 79.0 Length:193 Length:193
## Class :character 1st Qu.:127.0 Class :character Class :character
## Mode :character Median :185.0 Mode :character Mode :character
## Mean :189.3
## 3rd Qu.:246.0
## Max. :316.0
##
## Music.Emotion Age.Group Total.Looking.Time First.Face.Looking.Time
## Length:193 Min. :3.000 Min. : 1.654 Min. : 0.160
## Class :character 1st Qu.:3.000 1st Qu.:20.671 1st Qu.: 5.309
## Mode :character Median :6.000 Median :30.381 Median : 7.495
## Mean :6.093 Mean :29.196 Mean : 7.041
## 3rd Qu.:9.000 3rd Qu.:38.196 3rd Qu.: 9.185
## Max. :9.000 Max. :50.000 Max. :11.823
## NA's :3
4. Vérifiez à nouveau que vos données ne comportent pas de valeurs manquantes et que les données sont cohérentes.
sum(is.na(BabyData)) # Checking for missing values in the dataset
## [1] 0
summary(BabyData) # Viewing the summary of the dataset to check for inconsistencies
## Participant.ID Age.in.Days Condition Face.Race
## Length:193 Min. : 79.0 Length:193 Length:193
## Class :character 1st Qu.:127.0 Class :character Class :character
## Mode :character Median :185.0 Mode :character Mode :character
## Mean :189.3
## 3rd Qu.:246.0
## Max. :316.0
##
## Music.Emotion Age.Group Total.Looking.Time First.Face.Looking.Time
## Length:193 Min. :3.000 Min. : 1.654 Min. : 0.160
## Class :character 1st Qu.:3.000 1st Qu.:20.671 1st Qu.: 5.309
## Mode :character Median :6.000 Median :30.381 Median : 7.495
## Mean :6.093 Mean :29.196 Mean : 7.041
## 3rd Qu.:9.000 3rd Qu.:38.196 3rd Qu.: 9.185
## Max. :9.000 Max. :50.000 Max. :11.823
## NA's :0
5. Vérifiez la structure et assurez-vous que vos colonnes factorielles (Music.Emotion, Face.Race et Condition) sont correctement configurées.
str(BabyData)
## 'data.frame': 190 obs. of 8 variables:
## $ Participant.ID : chr "HJOGM7704U" "JHSEG5414N" "OCQFX4970K" "KLDOF5559R" ...
## $ Age.in.Days : int 93 98 93 93 93 100 93 91 98 100 ...
## $ Condition : chr "Other-Race Happy Music" "Other-Race Happy Music" "Other-Race Happy Music" "Other-Race Happy Music" ...
## $ Face.Race : chr "African" "African" "African" "African" ...
## $ Music.Emotion : chr "happy" "happy" "happy" "happy" ...
## $ Age.Group : int 3 3 3 3 3 3 3 3 3 3 ...
## $ Total.Looking.Time : num 44 18.3 24.6 12.9 12.8 ...
## $ First.Face.Looking.Time: num 8.27 6.94 4.22 7.54 4.23 ...
BabyData$Face.Race <- as.factor(BabyData$Face.Race)
BabyData$Music.Emotion <- as.factor(BabyData$Music.Emotion)
BabyData$Condition <- as.factor(BabyData$Condition)
6. Vérifiez si votre modèle est équilibré ou déséquilibré.
table(BabyData$Age.Group, BabyData$Condition) #unbalanced design
##
## Other-Race Happy Music Other-Race Sad Music Own-Race Happy Music
## 3 16 12 12
## 6 15 19 19
## 9 14 17 17
##
## Own-Race Sad Music
## 3 17
## 6 15
## 9 17
7. Effectuez une régression linéaire multi-variable sur le temps de regard du premier visage en tant que variable prédite, avec le groupe, la race du visage et leurs interactions en tant que variables prédictives. Affichez le résultat.
lm_model1 <- lm(First.Face.Looking.Time ~ Age.Group*Face.Race, data = BabyData)
summary(lm_model1)
##
## Call:
## lm(formula = First.Face.Looking.Time ~ Age.Group * Face.Race,
## data = BabyData)
##
## Residuals:
## Min 1Q Median 3Q Max
## -7.4524 -1.4478 0.3645 2.0507 4.5670
##
## Coefficients:
## Estimate Std. Error t value Pr(>|t|)
## (Intercept) 5.50710 0.75573 7.287 8.75e-12 ***
## Age.Group 0.22815 0.11542 1.977 0.0496 *
## Face.RaceChinese -0.04233 1.05722 -0.040 0.9681
## Age.Group:Face.RaceChinese 0.05036 0.16071 0.313 0.7544
## ---
## Signif. codes: 0 '***' 0.001 '**' 0.01 '*' 0.05 '.' 0.1 ' ' 1
##
## Residual standard error: 2.658 on 186 degrees of freedom
## Multiple R-squared: 0.05411, Adjusted R-squared: 0.03885
## F-statistic: 3.546 on 3 and 186 DF, p-value: 0.01564
8. Effectuez une régression linéaire multivariable similaire à celle décrite dans la question précédente. La variable prédite doit être le temps total de recherche, avec comme prédicteurs le groupe d’âge, la race du visage, l’émotion musicale et leurs interactions.
lm_model2 <- model <- lm(Total.Looking.Time ~ Age.Group * Face.Race * Music.Emotion, data = BabyData)
summary(lm_model2)
##
## Call:
## lm(formula = Total.Looking.Time ~ Age.Group * Face.Race * Music.Emotion,
## data = BabyData)
##
## Residuals:
## Min 1Q Median 3Q Max
## -24.8431 -8.0316 -0.1786 8.2809 27.7472
##
## Coefficients:
## Estimate Std. Error t value
## (Intercept) 28.0472 4.5406 6.177
## Age.Group -0.5167 0.7144 -0.723
## Face.RaceChinese -11.5424 6.6960 -1.724
## Music.Emotionsad -15.2955 6.6960 -2.284
## Age.Group:Face.RaceChinese 3.0376 1.0229 2.970
## Age.Group:Music.Emotionsad 3.4057 1.0229 3.330
## Face.RaceChinese:Music.Emotionsad 26.8342 9.3820 2.860
## Age.Group:Face.RaceChinese:Music.Emotionsad -5.7421 1.4252 -4.029
## Pr(>|t|)
## (Intercept) 4.16e-09 ***
## Age.Group 0.47045
## Face.RaceChinese 0.08645 .
## Music.Emotionsad 0.02351 *
## Age.Group:Face.RaceChinese 0.00338 **
## Age.Group:Music.Emotionsad 0.00105 **
## Face.RaceChinese:Music.Emotionsad 0.00473 **
## Age.Group:Face.RaceChinese:Music.Emotionsad 8.22e-05 ***
## ---
## Signif. codes: 0 '***' 0.001 '**' 0.01 '*' 0.05 '.' 0.1 ' ' 1
##
## Residual standard error: 11.72 on 182 degrees of freedom
## Multiple R-squared: 0.1742, Adjusted R-squared: 0.1425
## F-statistic: 5.486 on 7 and 182 DF, p-value: 9.76e-06
9. Compte tenu de l’interaction significative à trois voies, effectuer des analyses de corrélation de Pearson pour examiner la relation linéaire entre le temps total passé à regarder un visage et l’âge du participant en jours dans chaque condition.
unique_conditions <- unique(BabyData$Condition) #Get unique conditions
correlation_results <- list() ## Initialize a list to store results
# Loop through each condition and perform Pearson correlation
for (condition in unique_conditions) {
# Subset data for the current condition
subset_data <- subset(BabyData, Condition == condition)
subset_data$Age.Group <- as.numeric(as.character(subset_data$Age.Group))
# Perform Pearson correlation
correlation_test <- cor.test(subset_data$Age.Group, subset_data$Total.Looking.Time, method = "pearson")
# Store the result
correlation_results[[condition]] <- correlation_test
}
# Print the results
correlation_results
## $`Other-Race Happy Music`
##
## Pearson's product-moment correlation
##
## data: subset_data$Age.Group and subset_data$Total.Looking.Time
## t = -0.64059, df = 43, p-value = 0.5252
## alternative hypothesis: true correlation is not equal to 0
## 95 percent confidence interval:
## -0.3799180 0.2020743
## sample estimates:
## cor
## -0.09722666
##
##
## $`Other-Race Sad Music`
##
## Pearson's product-moment correlation
##
## data: subset_data$Age.Group and subset_data$Total.Looking.Time
## t = 4.4535, df = 46, p-value = 5.356e-05
## alternative hypothesis: true correlation is not equal to 0
## 95 percent confidence interval:
## 0.3136678 0.7206311
## sample estimates:
## cor
## 0.5488839
##
##
## $`Own-Race Happy Music`
##
## Pearson's product-moment correlation
##
## data: subset_data$Age.Group and subset_data$Total.Looking.Time
## t = 3.8943, df = 46, p-value = 0.0003166
## alternative hypothesis: true correlation is not equal to 0
## 95 percent confidence interval:
## 0.2490419 0.6851408
## sample estimates:
## cor
## 0.4979416
##
##
## $`Own-Race Sad Music`
##
## Pearson's product-moment correlation
##
## data: subset_data$Age.Group and subset_data$Total.Looking.Time
## t = 0.25438, df = 47, p-value = 0.8003
## alternative hypothesis: true correlation is not equal to 0
## 95 percent confidence interval:
## -0.2466891 0.3149919
## sample estimates:
## cor
## 0.03707966
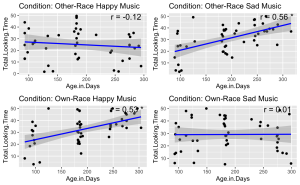
10. Visualisez la relation entre le temps total passé à regarder un visage et l’âge du participant en jours, en fonction des différentes conditions expérimentales. Chaque condition doit être représentée dans son propre panneau à l’intérieur d’une seule figure. En outre, pour chaque panneau :
# Get unique conditions
conditions <- unique(BabyData$Condition)
# Create a list to store plots
plot_list <- list()
# Loop through each condition and create a plot
for (condition in conditions) {
# Subset data for the condition
subset_data <- subset(BabyData, Condition == condition)
# Perform linear regression
fit <- lm(Total.Looking.Time ~ Age.in.Days, data = subset_data)
# Calculate Pearson correlation
cor_test <- cor.test(subset_data$Age.in.Days, subset_data$Total.Looking.Time)
# Create a scatter plot with regression line
p <- ggplot(subset_data, aes(x = Age.in.Days, y = Total.Looking.Time)) +
geom_point() +
geom_smooth(method = 'lm', color = 'blue') +
ggtitle(paste('Condition:', condition)) +
annotate("text", x = Inf, y = Inf, label = paste('r =', round(cor_test$estimate, 2), ifelse(cor_test$p.value < 0.05, "*", "")),
hjust = 1.1, vjust = 1.1, size = 5)
# Add plot to list
plot_list[[condition]] <- p
}
do.call(grid.arrange, c(plot_list, ncol = 2))
11. Analysez l’impact de la valence émotionnelle de la musique sur le temps de regard des visages de sa propre race et d’autres races dans différents groupes d’âge de nourrissons (3, 6 et 9 mois). Plus précisément, vous devez effectuer une série de tests t sur des échantillons indépendants.
# Ensure Age.Group is treated as a factor
BabyData$Age.Group <- as.factor(BabyData$Age.Group)
# Perform t-tests for each combination of Age.Group, Music.Emotion, and Face.Race
results <- list()
for(age_group in levels(BabyData$Age.Group)) {
for(music_emotion in unique(BabyData$Music.Emotion)) {
# Filter data for specific age group and music emotion
subset_data <- BabyData %>%
filter(Age.Group == age_group, Music.Emotion == music_emotion)
# Perform the t-test comparing Total.Looking.Time for own- vs. other-race faces
t_test_result <- t.test(Total.Looking.Time ~ Face.Race, data = subset_data)
# Store the results
result_name <- paste(age_group, music_emotion, sep="_")
results[[result_name]] <- t_test_result
}
}
# Print results
print(results)
## $`3_happy`
##
## Welch Two Sample t-test
##
## data: Total.Looking.Time by Face.Race
## t = -0.3153, df = 22.294, p-value = 0.7555
## alternative hypothesis: true difference in means between group African and group Chinese is not equal to 0
## 95 percent confidence interval:
## -12.465591 9.173257
## sample estimates:
## mean in group African mean in group Chinese
## 22.76875 24.41492
##
##
## $`3_sad`
##
## Welch Two Sample t-test
##
## data: Total.Looking.Time by Face.Race
## t = -1.0492, df = 22.86, p-value = 0.3051
## alternative hypothesis: true difference in means between group African and group Chinese is not equal to 0
## 95 percent confidence interval:
## -17.297369 5.658457
## sample estimates:
## mean in group African mean in group Chinese
## 21.32725 27.14671
##
##
## $`6_happy`
##
## Welch Two Sample t-test
##
## data: Total.Looking.Time by Face.Race
## t = 0.43226, df = 27.324, p-value = 0.6689
## alternative hypothesis: true difference in means between group African and group Chinese is not equal to 0
## 95 percent confidence interval:
## -6.401791 9.821475
## sample estimates:
## mean in group African mean in group Chinese
## 32.90100 31.19116
##
##
## $`6_sad`
##
## Welch Two Sample t-test
##
## data: Total.Looking.Time by Face.Race
## t = -0.62019, df = 27.075, p-value = 0.5403
## alternative hypothesis: true difference in means between group African and group Chinese is not equal to 0
## 95 percent confidence interval:
## -9.635393 5.162123
## sample estimates:
## mean in group African mean in group Chinese
## 30.20163 32.43827
##
##
## $`9_happy`
##
## Welch Two Sample t-test
##
## data: Total.Looking.Time by Face.Race
## t = -6.0414, df = 21.29, p-value = 5.08e-06
## alternative hypothesis: true difference in means between group African and group Chinese is not equal to 0
## 95 percent confidence interval:
## -27.28467 -13.31931
## sample estimates:
## mean in group African mean in group Chinese
## 19.13607 39.43806
##
##
## $`9_sad`
##
## Welch Two Sample t-test
##
## data: Total.Looking.Time by Face.Race
## t = 3.0179, df = 26.642, p-value = 0.005546
## alternative hypothesis: true difference in means between group African and group Chinese is not equal to 0
## 95 percent confidence interval:
## 3.335708 17.533234
## sample estimates:
## mean in group African mean in group Chinese
## 38.68853 28.25406
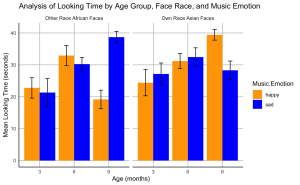
12. Créez un diagramme à barres pour visualiser les effets de la valence émotionnelle de la musique sur le temps de regard des nourrissons à différents âges pour les visages de leur propre race et ceux d’une autre race.
# Calculate means and standard errors
data_summary <- BabyData %>%
group_by(Age.Group, Face.Race, Music.Emotion) %>%
summarize(Mean = mean(Total.Looking.Time),
SE = sd(Total.Looking.Time)/sqrt(n())) %>%
ungroup()
## `summarise()` has grouped output by 'Age.Group', 'Face.Race'. You can override
## using the `.groups` argument.
# Create the bar plot
ggplot(data_summary, aes(x = factor(Age.Group), y = Mean, fill = Music.Emotion)) +
geom_bar(stat = "identity", position = position_dodge()) +
geom_errorbar(aes(ymin = Mean - SE, ymax = Mean + SE),
position = position_dodge(0.9), width = 0.25) +
scale_fill_manual(values = c("happy" = "orange", "sad" = "blue")) +
facet_wrap(~ Face.Race, scales = "free_x", labeller = labeller(Face.Race = c(Chinese = "Own Race Asian Faces", African = "Other Race African Faces"))) +
labs(x = "Age (months)", y = "Mean Looking Time (seconds)", title = "Analysis of Looking Time by Age Group, Face Race, and Music Emotion") +
theme_minimal() +
theme(
panel.grid.minor = element_blank(),
panel.grid.major = element_line(color = "gray", size = 0.5, linetype = "solid"), # Major grid lines
axis.line = element_line(color = "black", size = 0.5) # Axis lines
)
Bienvenue au laboratoire de perception et de sensorimotricité de l’université McMaster. En tant que psychologue cognitif en herbe, vous êtes sur le point d’entreprendre un voyage exploratoire sur l’effet de profondeur, un phénomène psychologique captivant qui suggère que les événements visuels se produisant à proximité (espace proche) sont traités plus efficacement que ceux qui sont plus éloignés (espace lointain). Cet effet offre une fenêtre unique sur l’architecture cognitive qui sous-tend nos expériences sensorielles, impliquant probablement l’implication du flux visuel dorsal, qui traite les relations spatiales et les mouvements dans l’espace proche, et le flux ventral, connu pour son rôle dans la reconnaissance d’informations visuelles détaillées.
Votre objectif est de déterminer si l’effet de profondeur est dépendant de la tâche, s’alignant strictement sur la dichotomie flux dorsal/flux ventral, ou s’il représente un avantage de traitement universel pour les stimuli dans l’espace proche à travers diverses tâches cognitives.
Votre parcours de recherche commence dans votre laboratoire. Imaginez le laboratoire comme une passerelle vers un monde tridimensionnel, où le concept de profondeur n’est pas seulement un sujet d’étude, mais aussi une expérience sensorielle vécue par vos participants ! Assis à l’intérieur d’une tente sombre, chaque participant tient un volant, son principal outil d’interaction et de saisie de réponses. Devant eux, un écran prend vie avec un environnement virtuel en 3D méticuleusement conçu pour tester les limites de la perception de la profondeur.
Le paysage virtuel auquel les participants sont confrontés est un modèle de simplicité et de complexité ; comme l’illustre la figure ci-dessous, devant les participants, un plan au sol s’étend dans la profondeur de l’écran, entrecoupé par deux séries de murs verticaux à des profondeurs variables – proches et éloignés. Les murs se trouvent de part et d’autre de l’axe central et se reflètent parfaitement sur la ligne médiane. Les textures du sol et des espaces réservés – une matrice de points aléatoires et un motif en damier, respectivement – conservent une densité constante. Ces indices visuels, ainsi que les gradients texturaux et la différence de taille rétinienne entre les objets proches et éloignés, agissent comme des repères subtils pour la perception de la profondeur.

De leur point de vue à la première personne, les participants sont invités à :
Grâce à cette expérience, vous ne vous contentez pas d’observer l’effet de profondeur ; vous le disséquerez, en découvrant les processus cognitifs qui permettent aux humains de naviguer dans la danse complexe de la profondeur dans notre vie quotidienne !
Commençons par charger les bibliothèques requises et le jeu de données. Pour ce faire, téléchargez le fichier “NearFarRep_Outlier.csv” et exécutez le code suivant.
# Loading the required
libraries library(tidyverse) # for data manipulation
library(rstatix) # for statistical analyses
library(emmeans) # for pairwise comparisons
library(afex) # for running anova using aov_ez and aov_car
library(kableExtra) # formatting html ANOVA tables
library(ggpubr) # for making plots
library(grid) # for plots
library(gridExtra) # for arranging multiple ggplots for extraction
library(lsmeans) # for pairwise comparisons
Lisez l’ensemble de données téléchargé “NearFarRep_Outlier.csv” en tant que “NearFarData”. N’oubliez pas de remplacer “path_to_your_downloaded_file” par le chemin réel de l’ensemble de données sur votre système.
NearFarData <- read.csv('path_to_your_downloaded_file/NearFarRep_Outlier.csv')
L’ensemble de données contient les temps de réponse des participants et comprend les colonnes suivantes :
Veuillez compléter les exercices ci-joints au mieux de vos capacités.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=156#h5p-4
1. Affichez les premières lignes pour comprendre votre ensemble de données. Affichez tous les noms de colonnes de l’ensemble de données.
head(NearFarData) #Displaying the first few rows## X ID Response Con TarRT
## 1 1 10 Loc Near 0.6200754
## 2 2 10 Loc Near 0.2219719
## 3 3 1 Loc Near 0.2270377
## 4 4 9 Loc Near 0.5270686
## 5 5 25 Loc Near 0.2272455
## 6 6 18 Loc Near 0.2292785
colnames(NearFarData)
## [1] "X" "ID" "Response" "Con" "TarRT"
2. Définissez “Response” et “Con” comme facteurs, puis vérifiez la structure de vos données pour vous assurer que vos facteurs et niveaux sont correctement définis.
NearFarData <- NearFarData %>% convert_as_factor(Response, Con)str(NearFarData)## 'data.frame': 11154 obs. of 5 variables:
## $ X : int 1 2 3 4 5 6 7 8 9 10 ...
## $ ID : int 10 10 1 9 25 18 4 9 8 18 ...
## $ Response: Factor w/ 2 levels "Disc","Loc": 2 2 2 2 2 2 2 2 2 2 ...
## $ Con : Factor w/ 2 levels "Far","Near": 2 2 2 2 2 2 2 2 2 2 ...
## $ TarRT : num 0.62 0.222 0.227 0.527 0.227 ...
3. Effectuer des contrôles de base des données pour vérifier les valeurs manquantes et la cohérence des données.
sum(is.na(NearFarData)) # Checking for missing values in the dataset## [1] 0
4. Convertissez les valeurs de votre colonne de mesures dépendantes “TarRT” en secondes.
NearFarData$TarRT <- NearFarData$TarRT * 1000
# Calculate means and standard errors for each combination of 'Response' and 'Con'summary_df <- NearFarData %>% group_by(Response, Con) %>% summarise( MeanRT = mean(TarRT), SERT = sd(TarRT) / sqrt(n()) )6. En utilisant le package “ggplot2”, créez un graphique linéaire avec des barres d’erreur pour la tâche de discrimination.
# Now, using ggplot to create the plotDisc.plot <- ggplot(data = filter(summary_df, Response=="Disc"), aes(x = Con, y = MeanRT, group = Response)) + geom_line(aes(linetype = "Discriminating")) + # Add a linetype aesthetic geom_errorbar(aes(ymin = MeanRT - SERT, ymax = MeanRT + SERT), width = 0.1) + geom_point(size = 3) + theme_gray() + labs( x = "Target Depth", y = "RT (ms)", color = "Experiment", linetype = "Experiment") + scale_linetype_manual(values = "dashed") + # Set the linetype for "Disc" to dashed ylim(630, 660) # Set the y-axis limits
7. De même, créez un graphique linéaire avec des barres d’erreur pour la tâche Localisation. Utilisez une ligne pointillée pour ce tracé, avec les exceptions suivantes :
Loc.plot <- ggplot(data = filter(summary_df, Response=="Loc"), aes(x = Con, y = MeanRT, group = Response)) +
geom_line(aes(linetype = "Localizing")) + # Add a linetype aesthetic
geom_errorbar(aes(ymin = MeanRT - SERT, ymax = MeanRT + SERT), width = 0.1) +
geom_point(size = 3) +
theme_gray() +
labs(
x = "Target Depth",
y = "RT (ms)",
color = "Experiment",
linetype = "Experiment") +
scale_linetype_manual(values = "solid") + # Set the line type for "Disc" to dashed
ylim(370, 410) # Set the y-axis limits
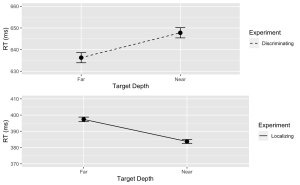
8. Enfin, utilisez la fonction grid.arrange() du package “gridExtra” pour superposer les tracés des tâches de discrimination et de localisation.
grid.arrange(Disc.plot, Loc.plot, ncol = 1) # Stack the plots on top of each other
9. À l’aide de la fonction “anova_test”, effectuez une ANOVA à deux voies entre sujets pour étudier les effets de Con (condition) et de Response (type de tâche) sur les temps de réponse cibles (TarRT). Après avoir exécuté l’ANOVA, utilisez la fonction “get_anova_table” pour présenter les résultats.
anova <- anova_test(
data = NearFarData, dv = TarRT, wid = ID,
between = c(Con, Response), detailed = TRUE, effect.size = "pes")
## Warning: The 'wid' column contains duplicate ids across between-subjects
## variables. Automatic unique id will be created
get_anova_table(anova)
## ANOVA Table (type III tests)
##
## Effect SSn SSd DFn DFd F p p<.05
## 1 (Intercept) 2.972143e+09 111582983 1 11150 296993.268 0.00e+00 *
## 2 Con 3.185839e+03 111582983 1 11150 0.318 5.73e-01
## 3 Response 1.762985e+08 111582983 1 11150 17616.741 0.00e+00 *
## 4 Con:Response 4.390483e+05 111582983 1 11150 43.872 3.67e-11 *
## pes
## 1 9.64e-01
## 2 2.86e-05
## 3 6.12e-01
## 4 4.00e-03
## Fitting a linear model to datalm_model <- lm(TarRT ~ Con * Response, data = NearFarData)
# Get the estimated marginal means
emm <- emmeans(lm_model, specs = pairwise ~ Con * Response)
# View the results
print(post_hoc_results)
## contrast estimate SE df t.ratio p.value
## Far Disc - Near Disc -11.5 2.70 11150 -4.250 0.0001
## Far Disc - Far Loc 238.9 2.67 11150 89.348 <.0001
## Far Disc - Near Loc 252.6 2.67 11150 94.581 <.0001
## Near Disc - Far Loc 250.4 2.69 11150 93.131 <.0001
## Near Disc - Near Loc 264.0 2.68 11150 98.341 <.0001
## Far Loc - Near Loc 13.6 2.66 11150 5.124 <.0001
##
## P value adjustment: tukey method for comparing a family of 4 estimates
Vous êtes chercheur au sein du laboratoire EdCog de l’Université McMaster. Le laboratoire mène une étude visant à comprendre les croyances des enseignants sur les capacités des étudiants dans les disciplines STIM (sciences, technologie, ingénierie et mathématiques). Cette étude est motivée par un nombre croissant de publications suggérant que les croyances des enseignants sur l’intelligence et la réussite – classées en croyances sur la brillance (l’idée que la réussite requiert un talent inné), croyances sur l’universalité (la croyance que la réussite est accessible à tous plutôt qu’à quelques privilégiés), et croyances sur l’état d’esprit (l’idée que l’intelligence et les compétences sont soit fixes, soit peuvent évoluer avec le temps) – jouent un rôle crucial dans les pratiques éducatives et les résultats des élèves. La compréhension de ces croyances est particulièrement importante dans les domaines des STIM, où les perceptions du talent inné par rapport aux compétences acquises peuvent influencer de manière significative les approches pédagogiques et l’engagement des étudiants.
L’enquête a été distribuée via LimeSurvey à des instructeurs des facultés de Sciences, de Sciences de la Santé et d’Ingénierie. Les participants ont été interrogés à travers une série de questions à l’échelle de Likert (allant de tout à fait en désaccord à tout à fait d’accord) visant à évaluer leurs croyances dans chacun des trois domaines. Des questions supplémentaires sur les données démographiques et le contexte ont été incluses pour contrôler des variables telles que les années d’expérience en enseignement, le domaine de spécialisation et le niveau d’éducation.
Le fichier de données d’échantillon (“EdCogData.xlsx”) pour cet exercice est structuré comme suit :
Commençons par exécuter le code suivant dans RStudio pour charger les bibliothèques requises. Assurez-vous de lire les commentaires intégrés tout au long du code pour comprendre ce que chaque ligne de code fait.
# Here we create a list called "my_packages" with all of our required libraries
my_packages <- c("tidyverse", "readxl", "xlsx", "dplyr", "ggplot2")
# Checking and extracting packages that are not already installed
not_installed <- my_packages[!(my_packages %in% installed.packages()[ , "Package"])]
# Install packages that are not already installed
if(length(not_installed)) install.packages(not_installed)
# Loading the required libraries
library(tidyverse) # for data manipulation
library(dplyr) # for data manipulation
library(readxl) # to read excel files
library(xlsx) # to create excel files
library(ggplot2) # for making plots
Assurez-vous d’avoir téléchargé l’ensemble de données requis (“EdCogData.xlsx”) pour cet exercice. Définissez le répertoire de travail de votre session R actuelle dans le dossier contenant l’ensemble de données téléchargé. Vous pouvez le faire manuellement dans le studio R en cliquant sur l’onglet “Session” en haut de l’écran, puis en cliquant sur “Set Working Directory”.
Si le fichier de données téléchargé et votre session R se trouvent dans le même dossier, vous pouvez choisir de définir votre répertoire de travail sur “l’emplacement du fichier source” (l’emplacement où votre session R actuelle est sauvegardée). S’ils se trouvent dans des dossiers différents, cliquez sur l’option “choisir un répertoire” et recherchez l’emplacement du jeu de données téléchargé.
Vous pouvez également effectuer cette opération en exécutant le code suivant :
setwd(file.choose())
Une fois que vous avez défini votre répertoire de travail manuellement ou par code, la console ci-dessous affiche le répertoire complet de votre dossier en sortie.
Lisez l’ensemble de données téléchargé en tant que “edcogData” et effectuez les exercices qui l’accompagnent au mieux de vos capacités.
# Read xlsx file
edcog = read_excel("EdCogData.xlsx")
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=161#h5p-5
Note : Les boîtes ombragées contiennent le code R, tandis que les boîtes blanches affichent la sortie du code, telle qu’elle apparaît dans RStudio. Le signe “#” indique un commentaire qui ne s’exécutera pas dans RStudio.
Chargez l’ensemble de données dans RStudio et inspectez sa structure.
head(edcogData) # View the first few rows of the datasetncol(edcogData) #Q1#[1] 26
colnames(edcogData) #Q2
#[1] "ID" "Brilliance1" "Brilliance2" "Brilliance3" "Brilliance4"
#[6] "Brilliance5" "MindsetGrowth1" "MindsetGrowth2" "MindsetGrowth3" "MindsetGrowth4"
#[11] "MindsetGrowth5" "MindsetFixed1" "MindsetFixed2" "MindsetFixed3" "MindsetFixed4"
#[16] "MindsetFixed5" "Nonuniversality1" "Nonuniversality2" "Nonuniversality3" "Nonuniversality4"
#[21] "Nonuniversality5" "Universality1" "Universality2" "Universality3" "Universality4"
#[26] "Universality5"
Préparez les données pour l’analyse en vous assurant qu’elles sont dans le bon format.
1. Y a-t-il des valeurs manquantes dans l’ensemble de données ?
sum(is.na(edcogData))
[1] 0
1. Créez des scores agrégés pour chaque dimension (Brilliance, Fixed, Growth, Nonuniversal, Universal).
edcogData$Brilliance <- rowMeans(edcogData[,c("Brilliance1", "Brilliance2", "Brilliance3", "Brilliance4", "Brilliance5")])
edcogData$Growth <- rowMeans(edcogData[,c("MindsetGrowth1", "MindsetGrowth2", "MindsetGrowth3", "MindsetGrowth4", "MindsetGrowth5")])
edcogData$Fixed <- rowMeans(edcogData[,c("MindsetFixed1", "MindsetFixed2", "MindsetFixed3", "MindsetFixed4", "MindsetFixed5")])
edcogData$Universal <- rowMeans(edcogData[,c("Universality1", "Universality2", "Universality3", "Universality4", "Universality5")])
edcogData$Nonuniversal <- rowMeans(edcogData[,c("Nonuniversality1", "Nonuniversality2", "Nonuniversality3", "Nonuniversality4", "Nonuniversality5")])
2. Créez un nouveau dataframe nommé “edcog.agg.wide” qui ne contient que la colonne ID et les colonnes de scores agrégés de “edcogData”.
edcog.agg.wide <- edcogData %>% select(ID, Brilliance, Fixed, Growth, Nonuniversal, Universal)
3. Convertissez “edcog.agg.wide” d’un format large à un format long nommé “edcog.agg.long”, avec les colonnes suivantes :
edcog.agg.long <- edcog.agg.wide %>%
select(ID, Brilliance, Fixed, Growth, Nonuniversal, Universal) %>%
pivot_longer(
cols = -ID, # Select all columns except for ID
names_to = "Dimension",
values_to = "AggregateScore" )
1. Créez un boxplot pour visualiser la distribution des scores agrégés à travers différentes dimensions (Brilliance, Fixed, Growth, Nonuniversal, Universal) à partir des données de l’enquête avec les spécifications suivantes :
ggplot(edcog.agg.long, aes(x = Dimension, y = AggregateScore, fill = Dimension)) +
geom_boxplot() +
scale_fill_manual(values = c("Brilliance" = "pink", "Fixed" = "yellow",
"Growth" = "green", "Nonuniversal" = "blue",
"Universal" = "purple")) +
labs(y = "Response (on a 1 to 5 scale)", x = "Dimension") +
theme_minimal() +
theme(legend.position = "none") # Hide the legend since color coding is evident
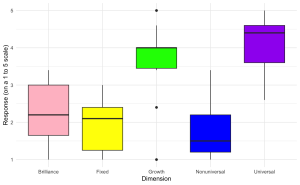
2. Générez un graphique de violon pour visualiser la distribution des scores agrégés pour différentes dimensions (Brilliance, Fixed, Growth, Nonuniversal, Universal) à partir des données de l’enquête avec les spécifications suivantes :
ggplot(edcog.agg.long, aes(x = Dimension, y = AggregateScore, fill = Dimension)) +
geom_violin(trim = FALSE) +
scale_fill_manual(values = c("Brilliance" = "pink", "Fixed" = "yellow",
"Growth" = "green", "Nonuniversal" = "blue",
"Universal" = "purple")) +
labs(y = "Response (on a 1 to 5 scale)", x = "Dimension") +
theme_minimal() + theme(legend.position = "none")
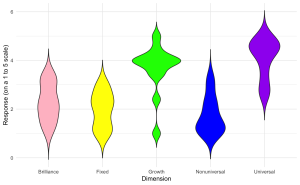
3. Améliorez le graphique de violon en superposant des points de données individuels pour montrer la distribution des données brutes en parallèle avec les estimations de densité agrégées.
ggplot(edcog.agg.long, aes(x = Dimension, y = AggregateScore, fill = Dimension)) +
geom_violin(trim = FALSE) +
geom_jitter(width = 0.1, size = 2, alpha = 0.5) + # Adjust 'width' for jittering, 'size' for point size, and 'alpha' for transparency
scale_fill_manual(values = c("Brilliance" = "pink", "Fixed" = "yellow",
"Growth" = "green", "Nonuniversal" = "blue",
"Universal" = "purple")) +
labs(y = "Response (on a 1 to 5 scale)", x = "Dimension") +
theme_minimal() +
theme(legend.position = "none")
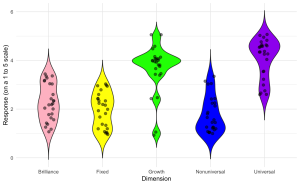
Assurez-vous d’avoir l’ensemble de données requis (“EdCogData.xlsx”) pour cet exercice téléchargé. Définissez le répertoire de travail de votre session R actuelle sur le dossier contenant l’ensemble de données téléchargé. Vous pouvez le faire manuellement dans R studio en cliquant sur l’onglet “Session” en haut de l’écran, puis en cliquant sur “Définir le répertoire de travail”.
Si le fichier de l’ensemble de données téléchargé et votre session R sont dans le même fichier, vous pouvez choisir l’option de définir votre répertoire de travail sur “l’emplacement du fichier source” (l’emplacement où votre session R actuelle est enregistrée). S’ils sont dans des dossiers différents, cliquez sur l’option “choisir le répertoire” et recherchez l’emplacement de l’ensemble de données téléchargé.
Vous pouvez également le faire en exécutant le code suivant :
Une fois que vous avez défini votre répertoire de travail soit manuellement, soit par code, dans la console ci-dessous, vous verrez le répertoire complet de votre dossier en sortie.
Lisez l’ensemble de données téléchargé en tant que “edcogData” et complétez les exercices d’accompagnement au mieux de vos capacités.
Vous êtes un chercheur clinique à l’Hôpital Général de Hamilton, et votre laboratoire étudie comment les gens vivent le deuil et font face à la perte d’un être cher. Plus précisément, certaines personnes ruminent lorsqu’elles sont en deuil, et votre laboratoire est donc intéressé à comprendre les différentes façons dont cette rumination liée au deuil se manifeste chez les gens. Andrews et al. (2021) ont récemment développé le Questionnaire d’Analyse de la Rumination en Deuil (BARQ) pour évaluer deux dimensions de la rumination : 1) la cause de la perte (c’est-à-dire, l’analyse des causes profondes – RCA) et 2) comment une personne réinvestit son temps de manière significative après la perte (c’est-à-dire, l’analyse du réinvestissement – RIA).
Votre laboratoire se pose les questions suivantes :
Comme Andrews et al. (2021), votre laboratoire décide de recueillir les informations suivantes à partir d’un questionnaire distribué à 50 répondants :
Pour répondre aux questions du laboratoire, veuillez exécuter les analyses suivantes.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-107
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-108
2. Effectuez une analyse factorielle confirmatoire (CFA) sur les sept éléments du BARQ. Les éléments 1 à 4 devraient former le facteur latent RCA, et les éléments 5 à 7 devraient former le facteur latent RIA.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-109
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-110
3. Comparez les moyennes des facteurs latents RCA et RIA entre les groupes suivants. Quelles comparaisons présentent des différences statistiquement significatives dans les moyennes de RCA et RIA ?
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-111
4. Les trois variables temporelles dans le questionnaire peuvent présenter une multilinéarité entre elles : l’âge du défunt, l’âge actuel du répondant et le temps écoulé depuis la mort. Par exemple, l’âge du défunt et l’âge du répondant peuvent être colinéaires, surtout si la relation du défunt au répondant est celle d’un enfant. Pour tester la multilinéarité, évaluez le facteur d’inflation de la variance (VIF) d’un modèle de régression qui inclut les trois variables temporelles comme prédicteurs pour RCA et RIA. Un VIF de 1 signifie qu’il n’y a pas de corrélation entre les variables prédicteurs, tandis qu’un VIF supérieur à 5 indique une forte corrélation.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-112
5. Créez un nuage de points du score du facteur latent RCA du participant (axe des y) par rapport à l’âge de l’enfant décédé (axe des x).
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=300#h5p-113
Andrews, P. W., Altman, M., Sevcikova, M., & Cacciatore, J. (2021). An evolutionary approach to grief-related rumination: Construction and validation of the Bereavement Analytical Rumination Questionnaire. Evolution and Human Behavior, 42(5), 441-452.
Les studios d’Hollywood et les producteurs de films sont vivement intéressés à déterminer quels types de scénarios résonneront avec le public et les critiques. Quelques scénaristes en herbe vous approchent, un chercheur en psychologie sociale spécialisé dans l’analyse de contenu qualitative, pour effectuer une analyse des intrigues de films afin de les aider à déterminer les types d’intrigues qui pourraient plaire aux téléspectateurs grand public. 150 films des cinq dernières années ont été sélectionnés au hasard et analysés pour leurs traits d’intrigue et de personnage. Vous décidez d’analyser les six caractéristiques narratives suivantes pour l’étude exploratoire : 1) le genre, 2) la forme de l’intrigue, 3) le type de but du protagoniste, 4) l’agence du protagoniste, 5) la coopérativité du protagoniste, et 6) l’assertivité du protagoniste. Vous êtes intéressé à voir comment ces caractéristiques se rapportent aux résultats suivants : 1) la note moyenne des critiques du film (en pourcentage) et 2) le bénéfice net du film (en dollars US).
Pour analyser ces six caractéristiques narratives, vous adoptez le schéma de Brown & Tu (2020) pour l’intrigue et le schéma de classification de Berry & Brown (2017) pour les personnages littéraires. Le schéma de codage pour les cinq caractéristiques narratives est le suivant :
| Étiquette | Code |
| Drame | 1 |
| Comédie | 2 |
| Romance | 3 |
| Action | 4 |
| Horreur | 5 |
| Étiquette | Code |
| Chute-Hausse | 1 |
| Chute-Hausse-Chute | 2 |
| Hausse-Chute | 3 |
| Hausse-Chute-Hausse | 4 |
| Étiquette | Code |
| Efforcement | 1 |
| Faire Face | 2 |
| Étiquette | Code |
| Haute | 1 |
| Moyenne | 2 |
| Basse | 3 |
| Étiquette | Code |
| Haute | 1 |
| Moyenne | 2 |
| Basse | 3 |
Vous recrutez également un deuxième codeur afin de déterminer s’il y a une fiabilité inter-juges dans votre méthode de codage.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-114
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-115
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-116
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-117
4. Visualisez ces distributions de formes d’intrigue dans chaque genre dans un graphique à barres groupées. Assurez-vous de bien étiqueter l’axe des y, l’axe des x et la légende.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-118
5. Effectuez des analyses comparatives pour voir si l’une des six caractéristiques est liée à une autre. Comme les six caractéristiques ne sont pas normalement distribuées, utilisez des tests non paramétriques, tels que le Chi-Carré. Par exemple, la relation entre le genre et l’intrigue est-elle statistiquement significative ?
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-119
6. Effectuez un test d’analyse de variance pour voir si l’une des cinq variables codées par l’évaluateur est liée à l’une des deux variables de résultat. Considérez si vous devez effectuer une ANOVA factorielle à 2 ou 3 voies. Quelles sont les hypothèses que vous devez considérer et tester avant de réaliser une ANOVA ?
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-120
7. Effectuez une analyse de regroupement pour voir si l’une des catégories des six variables de caractéristiques narratives se regroupe.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-121
8. Déterminez la fiabilité inter-juges entre les deux codeurs pour chacune des cinq variables codées par l’évaluateur. Un score de Kappa de Cohen supérieur à 0,8 reflète un fort accord inter-juges.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=302#h5p-122
Berry, M., & Brown, S. (2017). A classification scheme for literary characters. Psychological Thought, 10(2).
Brown, S., & Tu, C. (2020). The shapes of stories: A “resonator” model of plot structure. Frontiers of Narrative Studies, 6(2), 259-288.
Un nouveau jeu de rôle en ligne massivement multijoueur (MMORPG) de science-fiction a été lancé, permettant aux joueurs de concevoir le son de la voix de leur avatar. Le jeu propose une échelle de hauteur glissante pour que les joueurs puissent sélectionner la hauteur fondamentale (f0) et les fréquences formantiques (pf) (toutes deux mesurées en hertz) de la voix de leur avatar. Au fur et à mesure que les joueurs s’engagent dans le monde du jeu et interagissent avec d’autres joueurs à travers leur avatar, des traits de personnalité spécifiques pour leur avatar émergent. Afin de déterminer si les avatars créés dans ce monde de jeu de science-fiction ressemblent aux modèles vocaux et de personnalité trouvés dans le monde réel, les concepteurs du jeu ont collaboré avec des psychologues pour enquêter sur cette comparaison. Les concepteurs du jeu ont été particulièrement inspirés par l’étude de Stern et al. (2021) qui a exploré comment la hauteur de la voix est liée à l’extraversion, la dominance et la sociosexualité autodéclarées chez les hommes et les femmes.
L’étude actuelle sur les jeux vidéo a recruté un échantillon de 475 joueurs du jeu, 200 hommes et 275 femmes, tous âgés de 20 à 45 ans. Dans l’étude de Stern et al. (2021), les participants liraient de courts passages de texte afin que les chercheurs puissent déterminer la hauteur fondamentale et les fréquences formant la voix des participants. Cependant, les concepteurs du jeu sont en mesure d’extraire les informations sur la voix d’un avatar à partir des sélections que le joueur a faites sur l’échelle de hauteur glissante lorsqu’il a créé son avatar. Les concepteurs du jeu ont demandé aux 475 joueurs de remplir chacun un questionnaire sur les traits de personnalité de leur avatar (évaluations de Likert sur une échelle de 1 à 5 du Big 5), la dominance (évaluations de Likert sur une échelle de 1 à 5 de la Liste des adjectifs interpersonnels, et la sociosexualité (évaluations de Likert sur une échelle de 1 à 5 du SOI-R). Le score de sociosexualité est la moyenne des évaluations pour les trois dimensions de la sociosexualité : comportement, attitude et désir. Les concepteurs du jeu ont déjà calculé l’alpha de Cronbach pour les scores bruts des échelles et ont constaté qu’il y avait une bonne fiabilité. Comme certains MMORPG peuvent offrir la possibilité aux joueurs d’explorer et d’exprimer leur sexualité à travers leurs avatars, comme le nouveau MMORPG de science-fiction actuel qui est l’objet de ce scénario, les concepteurs du jeu sont curieux de savoir s’il existe une relation entre ces traits autodéclarés et le type de voix que le joueur a conçu pour son avatar.
Pour aider les concepteurs du jeu à enquêter sur cette question, veuillez répondre aux questions suivantes :
Chargez les données. Les données peuvent être trouvées dans voiceData.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=304#h5p-123
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=304#h5p-124
2. Créez des graphiques en violon comparant le sexe avec f0, pf, et les neuf variables de traits de personnalité. Inspectez visuellement les graphiques en violon et répondez aux questions suivantes:
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=304#h5p-125
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=304#h5p-126
Stern, J., Schild, C., Jones, B. C., DeBruine, L. M., Hahn, A., Puts, D. A., … & Arslan, R. C. (2021). Do voices carry valid information about a speaker’s personality?. Journal of Research in Personality, 92, 104092.
Vous êtes chercheur dans une académie de musique en Ontario. Vous souhaitez comprendre comment les musiciens d’un quatuor à cordes se coordonnent et se synchronisent entre eux. Pour ce faire, vous recrutez deux groupes de musiciens pour le laboratoire Large Interactive Virtual Environment (LIVELab, https://livelab.mcmaster.ca) à l’Université McMaster où les données comportementales en direct des musiciens peuvent être enregistrées. Plus précisément, le balancement du corps a été mesuré à l’aide d’un système de capture de mouvement optique infrarouge, qui nécessite que chaque musicien porte une casquette en feutre avec des marqueurs réfléchissants.
Les deux groupes de musiciens sont deux quatuors à cordes. Un quatuor à cordes se compose d’un premier violoniste (étiqueté M1), d’un deuxième violoniste (M2), d’un altiste (M3) et d’un violoncelliste (M4). Les deux quatuors à cordes ont interprété le même extrait musical de 2 minutes trois fois (c’est-à-dire trois essais). Un quatuor à cordes a interprété l’extrait dans la même pièce (la condition “vue”), tandis que l’autre quatuor à cordes a interprété dans une pièce où il y avait des séparateurs entre les musiciens pour les empêcher de se voir (la condition “pas de vue”).
Le balancement du corps a été mesuré comme le changement de position en millimètres dans la direction antéro-postérieure. Les données peuvent être trouvées [ICI]. Les mesures ont été prises à une fréquence de 8hz (c’est-à-dire 8 échantillons de temps par seconde). Un enregistrement de 2 minutes donnera donc 960 points de données d’échantillons de temps par musicien.
La synchronie musicale et la coordination interpersonnelle peuvent être analysées en comparant à quel point la série temporelle du balancement du corps d’un musicien est similaire à celle d’un autre musicien (c’est-à-dire une corrélation croisée entre deux séries temporelles) ainsi qu’à savoir si la série temporelle d’un musicien est capable de prédire la série temporelle d’un autre musicien (c’est-à-dire une analyse de causalité de Granger entre les séries temporelles), ce qui est également connu sous le nom de flux d’information.
En tant que chercheur de l’académie de musique, vous aimeriez comprendre les questions suivantes :
Est-ce que les quatuors à cordes dans les conditions de vue et de non-vue deviennent plus synchronisés à chaque essai successif ? Le quatuor à cordes dans la condition de soupir est-il plus synchronisé que le quatuor à cordes dans la condition de non-vue ? Est-ce que la série temporelle du premier violoniste “prévoit” la série temporelle des autres musiciens ? Pour répondre à la question ci-dessus, veuillez compléter les analyses statistiques suivantes :
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=307#h5p-127
2. Convertissez les données de la chronologie de chaque musicien en scores z.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=307#h5p-128
3. Exécutez une analyse de corrélation croisée de fenêtre entre les paires suivantes de musiciens dans chaque essai et dans chaque condition (il y a six combinaisons de paires possibles) :
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=307#h5p-129
4. Effectuez une analyse de causalité de Granger entre les paires suivantes de musiciens dans chaque essai et chaque condition (il y a 12 combinaisons de paires possibles)
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=307#h5p-130
5. En utilisant la modélisation à effets mixtes linéaires, déterminez si les corrélations croisées ont augmenté au fil des essais. Si c’est le cas, cela peut indiquer que le balancement du corps entre les musiciens devient plus similaire à mesure qu’ils se familiarisent avec la pièce.
Wood, E. A., Chang, A., Bosnyak, D., Klein, L., Baraku, E., Dotov, D., & Trainor, L. J. (2022). Creating a shared musical interpretation: Changes in coordination dynamics while learning unfamiliar music together. Annals of the New York Academy of Sciences, 1516(1), 106-113.
Vous êtes un chercheur en perceptions sociales et vous êtes intéressé par la question de savoir s’il existe des différences dans la façon dont les enfants du pays A et les enfants du pays B perçoivent la nationalité. Vous avez été spécifiquement inspiré par l’étude de Siddiqui, Cimpian et Rutherford (2020) comparant le degré de perspectives essentialistes des groupes nationaux entre les enfants canadiens et américains. Pour enquêter sur l’existence de différences dans les vues essentialistes sur les groupes nationaux, vous avez recruté 50 enfants âgés de 5 à 8 ans du pays A et 50 enfants âgés de 4 à 9 ans du pays B. Vous demandez aux enfants de répondre à des questions relatives aux catégories suivantes d’essentialisme :
Les options de réponse étaient binaires pour chaque question, où une réponse recevra un score de 1, tandis qu’une autre réponse recevra un score de zéro. Les questions dans la même catégorie ont été moyennées pour donner un score d’essentialisme pour cette catégorie. Les scores qui sont plus proches de 1 indiquent un essentialisme élevé. Les réponses des enfants peuvent être trouvées ci-dessous. Pour comparer si les vues essentialistes diffèrent entre les enfants du pays A et du pays B, veuillez exécuter les analyses statistiques suivantes :
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=309#h5p-131
2. Créez un graphique de dispersion pour montrer les scores d’essentialisme.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=309#h5p-132
3. Exécutez des comparaisons de tests t par paires entre les scores d’essentialisme pour chacune des sept catégories entre le pays A et le pays B.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=309#h5p-133
4. Comme il y a plusieurs comparaisons, le risque d’erreur de type 1 est augmenté. Exécutez une correction de Bonferroni pour prendre en compte cela.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=309#h5p-134
5. Créez un modèle linéaire à effets mixtes en utilisant les catégories d’essentialisme comme prédicteur catégoriel et l’âge des enfants comme prédicteur continu.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=309#h5p-135
Siddiqui, H., Cimpian, A., & Rutherford, M. D. (2020). Canadian children’s concepts of national groups: A comparison with children from the United States. Developmental psychology, 56(11), 2102.
II
L’électroencéphalogramme, ou EEG, est une technique de neuro-imagerie non invasive qui mesure et enregistre l’activité électrique du cerveau. Elle consiste à placer des électrodes sur le cuir chevelu pour détecter les fluctuations de tension résultant du courant ionique dans les neurones du cerveau. L’EEG fournit une représentation en temps réel de l’activité cérébrale et est largement utilisée en neurosciences informatiques pour étudier les processus neuronaux et comprendre le fonctionnement du cerveau.
En neurosciences informatiques l’analyse des données EEG se fait à l’aide d’algorithmes et de modèles mathématiques avancés afin d’extraire des informations précieuses sur les processus cognitifs, la perception sensorielle et divers troubles neurologiques. Les chercheurs utilisent l’EEG pour étudier les schémas d’activité neuronale, la connectivité cérébrale et la dynamique temporelle du traitement de l’information. La polyvalence et la précision temporelle de l’EEG en font un outil précieux pour étudier les fonctions cérébrales et contribuer à notre compréhension de l’interaction complexe des neurones dans le cerveau humain.
Les signaux EEG sont caractérisés par différentes bandes de fréquence qui reflètent l’activité neuronale sous-jacente. Les bandes de fréquences sont définies en fonction de la gamme de fréquences du signal EEG, et chaque bande est associée à un type spécifique d’activité cérébrale. Les bandes de fréquence sont les suivantes :
L’étude de l’interaction de ces bandes EEG fournit des informations précieuses sur le fonctionnement du cerveau, aidant les chercheurs et les cliniciens à comprendre les processus cognitifs, à diagnostiquer les troubles et à mettre au point des interventions thérapeutiques. L’analyse des données EEG permet d’explorer la dynamique cérébrale et peut ouvrir de nouvelles perspectives sur la complexité de l’esprit humain.
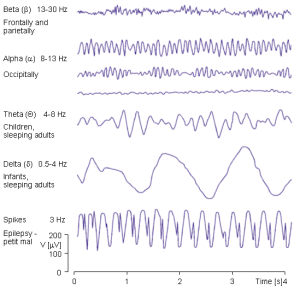
Dans les données EEG (électroencéphalographie), les canaux font référence aux endroits spécifiques du cuir chevelu où des électrodes sont placées pour enregistrer l’activité électrique produite par le cerveau. Ces électrodes font partie d’un capuchon ou d’un réseau EEG. Chaque canal correspond à une électrode unique, et les signaux recueillis à partir de ces canaux fournissent collectivement une vue d’ensemble de l’activité cérébrale.
L’emplacement des canaux est crucial pour la capture des signaux provenant des différentes régions du cerveau. Des normes internationales communes, telles que le système 10-20, sont utilisées pour définir l’emplacement de ces canaux. Ce système doit son nom au fait que la distance entre les électrodes adjacentes représente environ 20 % de la distance totale entre l’avant et l’arrière ou entre la droite et la gauche du crâne, en fonction de la région. Chaque canal enregistre les fluctuations de tension en temps réel, reflétant l’activité électrique des neurones dans la région cérébrale sous-jacente. L’analyse des données EEG provenant de plusieurs canaux permet aux chercheurs et aux cliniciens d’examiner la distribution spatiale de l’activité cérébrale et d’identifier les schémas associés à divers états cognitifs, troubles ou tâches spécifiques.
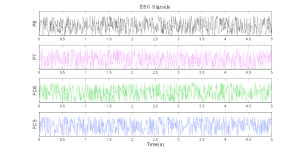
Dans cette section, nous nous concentrons sur l’analyse des données EEG à l’aide de R. Même si l’analyse des données EEG peut être effectuée à la fois avec MATLAB et R, et que le choix entre les deux dépend souvent des préférences du chercheur, de la disponibilité de boîtes à outils ou de packages spécifiques, et de la nature de l’analyse, MATLAB est un choix plus populaire pour l’analyse des données EEG en raison de sa large gamme de packages pour l’analyse des données EEG.
Les outils principaux pour R :
Il existe plusieurs outils pour prétraiter, visualiser et extraire des informations significatives des enregistrements EEG. Vous trouverez ci-dessous un bref aperçu des étapes typiques de l’analyse des données EEG à l’aide de R :
Des logiciels clés :
Prétraitement de l’EEG
Ce processus vise à éliminer le bruit, les artefacts et autres éléments indésirables tout en préservant l’intégrité des signaux neuronaux. Un prétraitement efficace garantit des résultats fiables lors des analyses ultérieures, en se concentrant sur l’activité neuronale réelle. Voici les principales étapes du prétraitement des données EEG :
En mettant en œuvre ces étapes de prétraitement, les chercheurs peuvent améliorer la qualité des données EEG, réduire le bruit et améliorer la précision des analyses ultérieures, ce qui permet d’obtenir des informations plus fiables sur les fonctions cérébrales et la cognition.
L’analyse statistique des données EEG (électroencéphalographie) est essentielle pour tirer des conclusions significatives des résultats expérimentaux. Les expériences EEG impliquent souvent la comparaison de conditions, de groupes ou de points dans le temps afin de découvrir des modèles d’activité cérébrale associés à des processus cognitifs spécifiques ou à des manipulations expérimentales. Voici un aperçu des principales considérations et méthodes d’analyse statistique des données EEG :
En utilisant ces approches statistiques, les chercheurs peuvent tirer des conclusions solides des données EEG, découvrir des modèles et élucider les mécanismes neurophysiologiques qui sous-tendent les processus cognitifs ou les conditions cliniques.
# Install eegkit package
install.packages("eegkit")
# Load eegkit package
library(eegkit)# Load EEG data
data("eegdata")
# View the first 5 rows of the data
head(eegdata)eegsmooth Lissage de l’électroencéphalographie (EEG) à un ou plusieurs canaux dans l’espace et/ou le temps.
## get "PZ" electrode of "c" subjects idx <- which(eegdata$channel=="PZ" & eegdata$group=="c") eegdata1 <- eegdata[idx,] ## Lissage temporaleegmod <- eegsmooth(eegdata1$voltage,time=eegdata1$time) ## Définir les données pour la prédiction time <- seq(min(eegdata1$time),max(eegdata1$time),length.out=100)yhat <- predict(eegmod,newdata=time,se.fit=TRUE) ## visualiser les résultats avec eegtime eegtime(time*1000/255,yhat$fit,voltageSE=yhat$se.fit,ylim=c(-4,4),main="Pz")
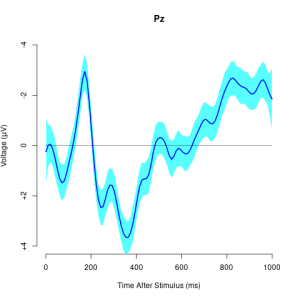 `eegtime` Creates plot of single-channel electroencephalography (EEG) time course with optional confidence
interval. User can control the plot orientation, line types, line colors, etc.
`eegtime` Creates plot of single-channel electroencephalography (EEG) time course with optional confidence
interval. User can control the plot orientation, line types, line colors, etc.Example: Plotting a single channel
## get "PZ" electrode from "eegdata" data
idx <- which(eegdata$channel=="PZ")
eegdata2 <- eegdata[idx,]
## get average and standard error (note se=sd/sqrt(n))
eegmean <- tapply(eegdata2$voltage,list(eegdata2$time,eegdata2$group),mean)
eegse <- tapply(eegdata2$voltage,list(eegdata2$time,eegdata2$group),sd)/sqrt(50)
## plot results with legend
tseq <- seq(0,1000,length.out=256)
eegtime(tseq,eegmean[,2],voltageSE=eegse[,2],ylim=c(-10,6),main="Pz")
eegtime(tseq,eegmean[,1],vlty=2,vcol="red",voltageSE=eegse[,1],scol="pink",add=TRUE)
legend("bottomright",c("controls","alcoholics"),lty=c(1,2),
lwd=c(2,2),col=c("blue","red"),bty="n") 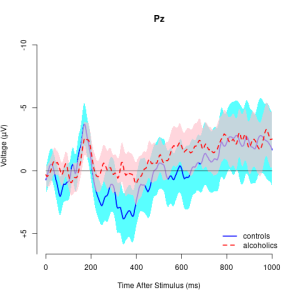
Dans une étude portant sur des enregistrements EEG, les données de 10 alcooliques et de 10 sujets témoins ont été recueillies au cours d’une expérience de 10 secondes. L’ensemble de données comprend quatre colonnes : “ID”, “Groupe”, “Temps” et “Tension”.
Analyse exploratoire en R
Analyse statistique en R
Effectuez les analyses suivantes à l’aide des données chargées :
Cette étude vise à explorer et à analyser statistiquement les données EEG afin de déterminer s’il existe des différences perceptibles dans les niveaux de tension entre les alcooliques et les sujets témoins. La combinaison de la visualisation exploratoire et des tests statistiques permet une compréhension globale des schémas EEG et des distinctions potentielles entre les groupes.
L’imagerie par résonance magnétique (IRM) est une technique d’imagerie médicale essentielle qui utilise la résonance magnétique nucléaire pour produire des structures internes détaillées du corps, particulièrement efficaces pour visualiser les tissus mous avec une clarté supérieure à celle des rayons X ou des tomodensitogrammes. Cette modalité est largement utilisée pour diagnostiquer un large éventail d’affections, notamment l’imagerie cérébrale pour détecter les tumeurs, les accidents vasculaires cérébraux et d’autres affections neurologiques.
L’IRM implique que le patient soit allongé à l’intérieur d’un grand aimant, où des ondes radio ciblent le corps. Les capteurs de l’IRM détectent l’énergie émise par le corps et convertissent ces données en images. Contrairement aux méthodes faisant appel aux rayonnements ionisants, le profil de sécurité de l’IRM permet une utilisation répétée. Toutefois, son champ magnétique puissant peut être contre-indiqué chez les patients porteurs d’implants métalliques spécifiques, et certains peuvent trouver la procédure longue et immobile difficile.
Dans le domaine des neurosciences, les capacités d’imagerie non invasives et détaillées de l’IRM sont indispensables pour distinguer avec précision les tissus cérébraux et détecter les anomalies, jouant ainsi un rôle essentiel dans le diagnostic et le suivi de maladies neurologiques telles que la sclérose en plaques et la maladie d’Alzheimer.
Dans cette section, nous nous concentrons sur la visualisation et l’analyse des données d’IRM à l’aide de la programmation R.
Format des données :
Les images IRM sont généralement disponibles au format NIFTI, avec des extensions de fichier telles que .nii ou .nii.gz (compressé). Les fichiers NIFTI sont compatibles avec divers logiciels d’analyse en neuroimagerie.
Progiciels R clés :
Chargement de données IRM dans R :
# Loading the oro.nifti and neurobase packages
library(oro.nifti)
library(neurobase)
# Reading a NIFTI file
mri_img = readnii("training01_01_mri_img.nii.gz")Visualiser les données de l’IRM
ortho2(mri_img)cette fonction de neurobase montre un objet nifti en 3 plans.
image(mri_img, useRaster= TRUE)Cette fonction de oro.nifti offre une vue en boîte lumineuse montrant toutes les planches de l’IRM.
oro.nifti::slice(mri_img, z = c(60, 80))Est nécessaire pour l’examen détaillé de certaines structures neuroanatomiques
Analyse des distributions des valeurs des voxels :
En IRM, les voxels (abréviation de “pixels volumétriques”) fonctionnent de la même manière que les pixels des images 2D, mais ils représentent les plus petites unités tridimensionnelles distinguables du volume scanné.
Les valeurs des voxels dans les données d’IRM peuvent être analysées pour comprendre la distribution des différents types de tissus
plot(density(mri_img))hist(mri_img)La segmentation des régions du cerveau :
Un aspect essentiel de l’analyse IRM en neurosciences c’ est la segmentation du cerveau en régions d’intérêt biologiquement significatives (ROI). Cela comprend la segmentation des tissus, l’identification des structures de la matière grise profonde et la segmentation des pathologies telles que les lésions de sclérose en plaques ou les tumeurs.
Pour des informations plus détaillées et des techniques avancées d’analyse d’IRM à l’aide de R, les ressources suivantes sont recommandées :
Le prétraitement est une étape critique de l’analyse des images IRM, essentielle pour garantir la précision et la fiabilité des résultats. Ce processus comprend plusieurs étapes clés :
Le prétraitement améliore la qualité de l’image, l’interprétabilité et la puissance statistique des analyses. Il prépare le terrain pour des analyses avancées, y compris des études d’IRM fonctionnelle et des approches d’apprentissage automatique.
Bien que le prétraitement soit essentiel, il n’est pas l’objet de ce tutoriel. Pour obtenir des méthodes détaillées de prétraitement des images IRM dans R, nous vous recommandons vivement de consulter ce tutoriel tutorial de John Muschelli et Kristin Linn.
Pour les besoins de ce tutoriel, nous supposerons que le prétraitement est déjà terminé.
L’analyse statistique des données d’IRM comprend une variété de techniques, chacune offrant un aperçu unique de la structure et de la fonction du cerveau :
La morphométrie basée sur les voxels est une technique populaire dans l’analyse IRM. Ce processus consiste à se concentrer sur des régions d’intérêt spécifiques (ROI) dans le cerveau et à analyser le volume de ces régions. Le volume d’une région peut être calculé en multipliant le nombre de voxels dans la région par le volume de chaque voxel.
Bien que notre objectif principal ne soit pas de calculer le volume d’une zone d’intérêt, les personnes intéressées peuvent suivre les étapes suivantes pour masquer une zone d’intérêt et calculer son volume. Notez que ces étapes nécessitent des logiciels et des bibliothèques spécifiques.
Assurez-vous que les progiciels nécessaires sont installés. L’installation d’ANTsR est plus complexe que celle des paquets R habituels. Vous trouverez des instructions d’installation détaillées ici.
library(ANTsR)
library(oro.nifti)mri_image <- niftiImageRead("path_to_your_mri_image.nii", reorient = FALSE)segmentation_results <- atropos(a = mri_image, m = '[3,1x1x1]', c = '[2,0]', i = 'kmeans[3]', x = 1)csf <- segmentation_results$segmentation == 1
gm <- segmentation_results$segmentation == 2
wm <- segmentation_results$segmentation == 3
niftiImageWrite(csf, "csf_segmented.nii")
niftiImageWrite(gm, "gm_segmented.nii")
niftiImageWrite(wm, "wm_segmented.nii")vres = voxres(t1, units = "cm")
vol_csf = csf * vresPrenons l’exemple d’une étude portant sur 30 adultes de plus de 55 ans atteints de la maladie d’Alzheimer et 30 témoins. L’étude s’étend sur 2 ans et suit les changements de volume de l’hippocampe.
Effectuez les analyses suivantes sur les données que vous avez chargées à votre environnement d’analyse:
1. Représentation graphique des moyennes marginales de diagnostic: visualiser la perte moyenne du volume de l’hippocampe chez les patients atteints de la maladie d’Alzheimer par rapport au groupe de contrôle.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=181#h5p-7
2. Analyse de la variance (ANOVA) : Effectuez une ANOVA pour évaluer l’effet de la maladie d’Alzheimer sur la perte de volume. Cette analyse permettra de déterminer si la perte de volume est significativement différente entre les patients atteints de la maladie d’Alzheimer et le groupe de contrôle.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=181#h5p-8
3. Defi – l’analyse de la covariance (ANCOVA) : En tant que défi avancé, utilisez l’ANCOVA pour évaluer l’effet de la maladie d’Alzheimer sur la perte de volume tout en contrôlant l’association linéaire entre la perte de volume et le volume initial. Cette analyse tient compte du volume initial de l’hippocampe, ce qui permet de mieux comprendre l’impact de la maladie.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=181#h5p-9
Cette étude de cas fournit une application pratique du traitement d’images IRM et de l’analyse statistique en R, démontrant la puissance de ces techniques dans la compréhension de conditions neurologiques complexes telles que la maladie d’Alzheimer.
L’imagerie par résonance magnétique fonctionnelle (IRMf) est une technique de neuro-imagerie non invasive qui a révolutionné notre compréhension du cerveau. Elle est principalement utilisée pour observer et mesurer l’activité cérébrale et constitue un outil précieux pour la recherche en neurosciences. Elle est principalement utilisée pour observer et mesurer l’activité cérébrale, ce qui en fait un outil précieux pour la recherche en neurosciences. L’IRMf fonctionne selon le principe que le flux sanguin cérébral et l’activation neuronale sont couplés. Lorsqu’une zone du cerveau est plus active, elle consomme plus d’oxygène et, pour répondre à cette demande accrue, le flux sanguin vers la zone active augmente également. Ce phénomène est connu sous le nom de réponse hémodynamique.
Le prétraitement des données IRMf est essentiel pour améliorer la qualité des données, normaliser les données d’une session à l’autre et d’un sujet à l’autre, supprimer les artefacts dus aux mouvements du sujet et aux processus physiologiques, et optimiser l’interprétation du signal BOLD, garantissant ainsi la précision et la fiabilité des analyses ultérieures.
Dans cette section, nous nous concentrerons sur la manière dont vous pouvez visualiser et travailler avec des données d’IRMf dans R.
Bien que les données d’IRMf puissent être enregistrées dans des formats bruts tels que DICOM ou PAR/REC spécifique au scanner, les types les plus courants pour l’analyse sont les formats traités tels que le NIfTI, largement utilisé, qui stocke les données et informations sur le volume cérébral, et BIDS, une structure de répertoire standardisée facilitant le partage des données et la compatibilité avec divers outils d’analyse. Le choix du bon type dépend de l’étape de l’analyse et des besoins de compatibilité, mais NIfTI et BIDS sont généralement préférés pour les données traitées en raison de leur flexibilité et de leur adoption généralisée. Pour ce tutoriel, nous utilisons les formats de fichiers NIFTI.
Vous pouvez télécharger ici un exemple de données IRMf enregistrées au format NIFTI.
1. Chargement des progiciels necessaires :
install.packages(c("oro.nifti", "fmri", "neurobase", "fslr"))
library(oro.nifti)
library(fmri)
library(neurobase)
library(fslr)2. Chargement des donnees d’IRMf :
# Load a NIfTI file
fmri_data <- readNIfTI("path/to/your/fmri.nii")
# Check the dimensions and structure
dim(fmri_data) # Check dimensions (x, y, z, time)
# As you can see fMRI has 4 dimensions which are 3D space + time.
str(fmri_data) # View data structure3. Visualisation des donnees d’IRMf :
# Display a single slice
ortho2(fmri_data, xyz = c(40, 40, 20)) # Visualize slice at coordinates (40, 40, 20)# Extract time series from a specific voxel.
voxel_time_series <- fmri_data[25, 30, 15, ]
# Plot the time series
plot(voxel_time_series, type = "l", xlab = "Time", ylab = "BOLD Signal")Dans une étude de neuro-imagerie, une expérience d’IRMf a été menée pour étudier les réponses du cerveau à des stimuli visuels. L’étude a utilisé un paradigme en blocs dans lequel les participants ont vu des images d’un bébé à des intervalles fixes. Plus précisément, chaque participant a été exposé à l’image d’un bébé pendant 15 secondes, suivies d’un intervalle de 15 secondes pendant lequel aucune image n’était affichée (écran noir). Cette séquence a été répétée pendant 10 cycles, soit une durée totale de l’expérience de 300 secondes, ou 5 minutes.
L’ensemble de données voxels.csv qui l’accompagne contient des séries temporelles de données provenant de 10 voxels cérébraux sélectionnés d’un participant, fournissant un aperçu ciblé de l’activité cérébrale localisée au cours de l’expérience. Les données sont structurées de manière à faciliter l’analyse des schémas de réponse du cerveau en relation avec le stimulus visuel. En outre, l’ensemble de données comprend une colonne de stimuli qui indique le moment où les stimuli visuels ont été présentés au participant. Dans cette colonne, une valeur de 1 indique la présence de l’image du bébé à l’écran, tandis qu’une valeur de 0 indique une phase où aucune image n’a été montrée (écran noir). Les données de l’IRMf ont été enregistrées toutes les secondes, il y a donc 300 pas de temps dans les données.
Certainement ! Voici quelques questions que vous pourriez poser aux étudiants en rapport avec chaque partie du code R fourni, afin de tester leur compréhension de l’analyse et de la visualisation des données en R :
Pour des informations plus détaillées et des techniques avancées d’analyse statistique de l’IRMf à l’aide de R, les ressources suivantes sont recommandées :
Vous êtes-vous déjà demandé comment interpréter un ensemble de données ? Parfois, les ensembles de données sont disponibles mais dans des formats qui semblent déroutants ? Parfois, le format d’organisation dans lequel vous recevez un ensemble de données n’a pas beaucoup de sens et n’est pas très utile pour vous renseigner sur les données. Pour obtenir des informations sur vos données, vous devez parfois utiliser des outils d’organisation des données – en R, nous appelons cette série d’outils “data wrangling”.
En chargeant la série de paquets tidyverse – un groupe de paquets (tidyr, dplyr et ggplot2), nous pouvons facilement organiser, ordonner et visualiser nos données afin de vérifier qu’elles sont organisées dans des formats raisonnables.
Dans cet article, nous allons passer en revue quelques-unes des opérations de base de tidyverse qui sont parmi les plus utilisées, et les utiliser pour manipuler un ensemble de données catégoriques afin de présenter l’information de manière succincte.
Quelques ressources pratiques : voici quelques feuilles de contrôle pour les notions de base pour le nettoyage et le traitement des données dans RStudio en utilisant la série de paquets tidyverse (N.B. ces feuilles de contrôle sont développés par posit) :
Data Wrangling : https://www.rstudio.com/wp-content/uploads/2015/02/data-wrangling-cheatsheet.pdf
Tidyr : https://bioinformatics.ccr.cancer.gov/docs/rintro/resources/tidyr_cheatsheet.pdf
Dplyr : https://nyu-cdsc.github.io/learningr/assets/data-transformation.pdf
library(tidyverse) # core series of data wrangling packages.
library(dplyr) # core data wrangling grammar
library(ggplot2) # data visualisation tools
library(RColorBrewer) # colour palettes
library(here) # file directories
library(gridExtra) # arranging plots Les données utilisées pour cette série d’exercices tidyverse proviennent du dépôt de données d’apprentissage automatique de l’Université de Californie à Irvine (UC Irvine Machine learning). Des informations sommaires sur l’ensemble de données et les variables qu’il contient sont disponibles sur le lien suivant : https://archive.ics.uci.edu/dataset/915/differentiated+thyroid+cancer+recurrence
D’autres informations sur l’ensemble de données et son utilisation sont disponibles dans le document source
Borzooei, S., Briganti, G., Golparian, M. et al. Machine learning for risk stratification of thyroid cancer patients: a 15-year cohort study. Eur Arch Otorhinolaryngol (2023). https://doi.org/10.1007/s00405-023-08299-w
Chargez ci-dessous une copie de l’ensemble de données sur le cancer de la thyroïde et imprimez l’en-tête (les 6 premières rangées).
thyroid.data <- read.csv("Thyroid_Diff.csv")
print (head(thyroid.data))
export.path <- here::here("/Tidyverse_DataWrangling")Les cadres de données ont une structure définie et une certaine terminologie est utilisée pour décrire les différentes structures que peuvent prendre les cadres de données.
Si vous regardez le cadre de données sur le cancer de la thyroïde, le cadre de données est-il ordonné ? Le cadre de données est-il long ou large ?
Pour plus d’informations sur la manipulation des données et les opérations à travers le tidyverse, vous pouvez consulter ce chapitre du livre en ligne R for Data Science : 2e (dont certaines informations ont été utilisées pour construire ces activités) : https://r4ds.hadley.nz/data-transform
view(thyroid.data)
# the dataframe is tidy and in a wide format - wrangling will be needed to present informative counts from within the dataframe Lorsque vous regardez le cadre de données thyroid.data, chaque colonne décrit quelque chose sur chaque patient et sur le cancer de la thyroïde qui lui est associé. Mais comment interpréter les tendances ou visualiser facilement les informations contenues dans le cadre de données ? Pour ce faire, vous devrez faire un peu de ce que nous appelons le traitement des données. Il s’agit d’organiser et de modifier la structure de votre cadre de données afin de présenter des informations pertinentes par le biais de statistiques ou de visualisations succinctes et ciblées.
Si vous imprimez les noms des colonnes, vous verrez qu’il y a beaucoup de caractéristiques catégorielles différentes qui décrivent le patient et son cancer. Comment visualiser des données catégorielles de manière à présenter des nombres ou des proportions basés sur ces variables catégorielles ? Cette activité de manipulation de données vous aidera à y parvenir. En route pour le tidyverse ! 🙂 .
colnames ( thyroid.data)La première chose à comprendre est l’opérateur pipe %>%. Ce petit champion de la manipulation de données vous permet d’écrire proprement et d’enchaîner une série d’opérations de manipulation de données afin d’effectuer de manière transparente une série de manipulations de données pour produire la structure souhaitée de l’image de données avec les colonnes et les lignes nécessaires pour produire les visualisations qui présentent le mieux les informations contenues dans l’image de données.
Tout d’abord, l’opérateur pipe peut être appliqué aux vecteurs ainsi qu’aux cadres de données. De la même manière que nous pouvons “canaliser” les sorties de vecteurs dans des opérations, nous pouvons “canaliser” des colonnes ou des cadres de données entiers dans des fonctions de manipulation de données afin de produire la structure de données requise.
Pour commencer la prochaine série de questions, vous devrez être à l’aise avec l’opérateur pipe pour manipuler vos données à partir du cadre de données sur le cancer de la thyroïde que vous avez chargé dans RStudio. La première activité consiste à manipuler le cadre de données pour compter le nombre de cas de cancer de la thyroïde pour chacune des quatre pathologies différentes de l’ensemble de données.
## ------------------------------------------------------- ##
#### Using the pipe operator to pass inputs to functions ####
## ------------------------------------------------------- ##
# give this code and make it visible to the students
# try computing the mean of a vector of numbers :
no.piped.mean <- mean(c(1,2,3,4,5,6,7,8,9, 10, 11, 12))
piped.mean <- c(1,2,3,4,5,6,7,8,9,10,11, 12) %>% mean()
print (paste("mean without pipe operator: ", no.piped.mean,
"mean with pipe operator: ", piped.mean))
## --------- wrangling the thyroid cancer dataframe ---------- ##
## --------------------------------------------- ##
##### 1. grouping thyroid cancer by pathology #####
## --------------------------------------------- ##
# this is the first step to organizing the dataframe for downstream analysis
# the pipe operator is taking the thyroid.data dataframe and applying the group_by function to it grouping rows together based on the values in the pathology column of the dataframe.
thyroid.by.pathology <- thyroid.data %>% group_by(Pathology)
print (head(thyroid.by.pathology))
## ----------------------------------------------- ##
##### 2. summarise the counts of each pathology #####
## ----------------------------------------------- ##
# now you can prepare a frequency table - of all the cases in this thyroid cancer dataset, how many cases are of EACH pathology?
# this step "pipes" the thyroid.by.pathology dataframe produced in the previous step, to the summarise function, counting the frequency of each pathology across the entire dataset
pathology.frequencies<- thyroid.by.pathology %>% summarise (Frequency = n())
print (head(pathology.frequencies))Cet ensemble de données contient 4 pathologies cancéreuses uniques : Folliculaire, Cellule de Hurthel, Micropapillaire et Papillaire. Combien de cas de chaque type se trouvent dans cet ensemble de données ? Présentez vos résultats sous la forme d’un histogramme de fréquence. Annotez les barres de l’histogramme de fréquence pour indiquer le nombre de cas dans chaque pathologie.
Conseil : utilisez la série de packages tidyverse pour manipuler vos données.
# Use dplyr to group by Pathology and count the number of occurrences
# this time all the steps outlined in the preliminary code chunk was piped together and brought together to produce a pathology frequency dataframe.
pathology_freq <- thyroid.data %>%
group_by(Pathology) %>%
summarise(Frequency = n())
# Print the frequency distribution
print(pathology_freq)
# Use ggplot2 to create a bar plot of the frequency histogram.
thyroid.cancer.freqplot <- ggplot(pathology_freq, aes(x = Pathology, y = Frequency)) +
geom_bar(stat = "identity", fill = "lightsteelblue3") +
geom_text(aes(label = Frequency), vjust = 1.5, hjust = 0.5) +
theme(axis.text.x = element_text(angle = 45, hjust = 1)) +
theme_classic()+
labs(x = "Pathology", y = "Frequency", title = "Frequency Distribution : Pathology Categories")
# plot inspection
print (thyroid.cancer.freqplot)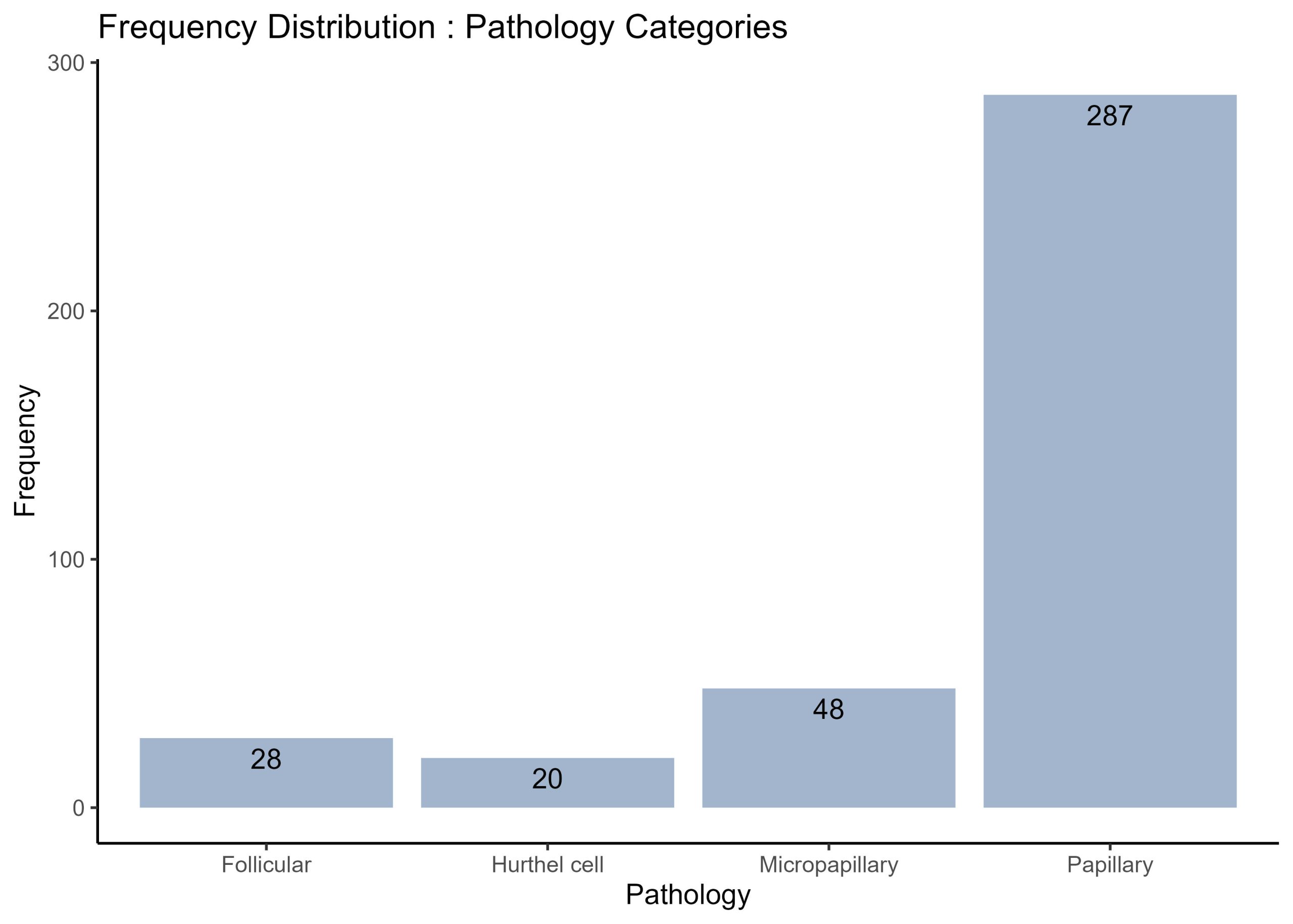
Le premier histogramme de fréquence est intéressant car il permet de visualiser facilement le nombre de cas de chaque type de pathologie cancéreuse dans l’ensemble de données, mais il est important de noter qu’il existe d’autres données sur les patients qui sont également précieuses, mais qui ne sont pas présentes dans la visualisation précédente. Supposons que vous souhaitiez également connaître le nombre d’hommes et de femmes pour chaque pathologie. Comment obtiendrez-vous les proportions d’hommes et de femmes pour chaque pathologie et comment modifieriez-vous l’histogramme de fréquence ci-dessus pour visualiser le nombre d’hommes et de femmes pour chaque groupe de pathologie ?
Modifiez l’histogramme de fréquence ci-dessus pour montrer les proportions d’hommes et de femmes dans chaque pathologie, et annotez chaque barre avec les nombres d’hommes et de femmes dans chaque groupe de pathologie.
# Group by Pathology and Gender, and count the number of occurrences
gender_pathology_freq <- thyroid.data %>%
group_by(Pathology, Gender) %>%
summarise(Frequency = n())
# Plot the stacked bar chart
thyroid.freqplot.by.Gender <- ggplot(gender_pathology_freq, aes(x = Pathology, y = Frequency, fill = Gender)) +
geom_bar(stat = "identity") +
geom_text(aes(label = Frequency), position = position_stack(vjust = 0.5)) +
theme(axis.text.x = element_text(angle = 45, hjust = 1)) +
theme_classic()+
labs(x = "Pathology", y = "Frequency", fill = "Gender", title = "Frequency Distribution of Each Pathology Category by Gender") # set the fill of each bar to show the proportions of genders
# plot inspection step
print (thyroid.freqplot.by.Gender)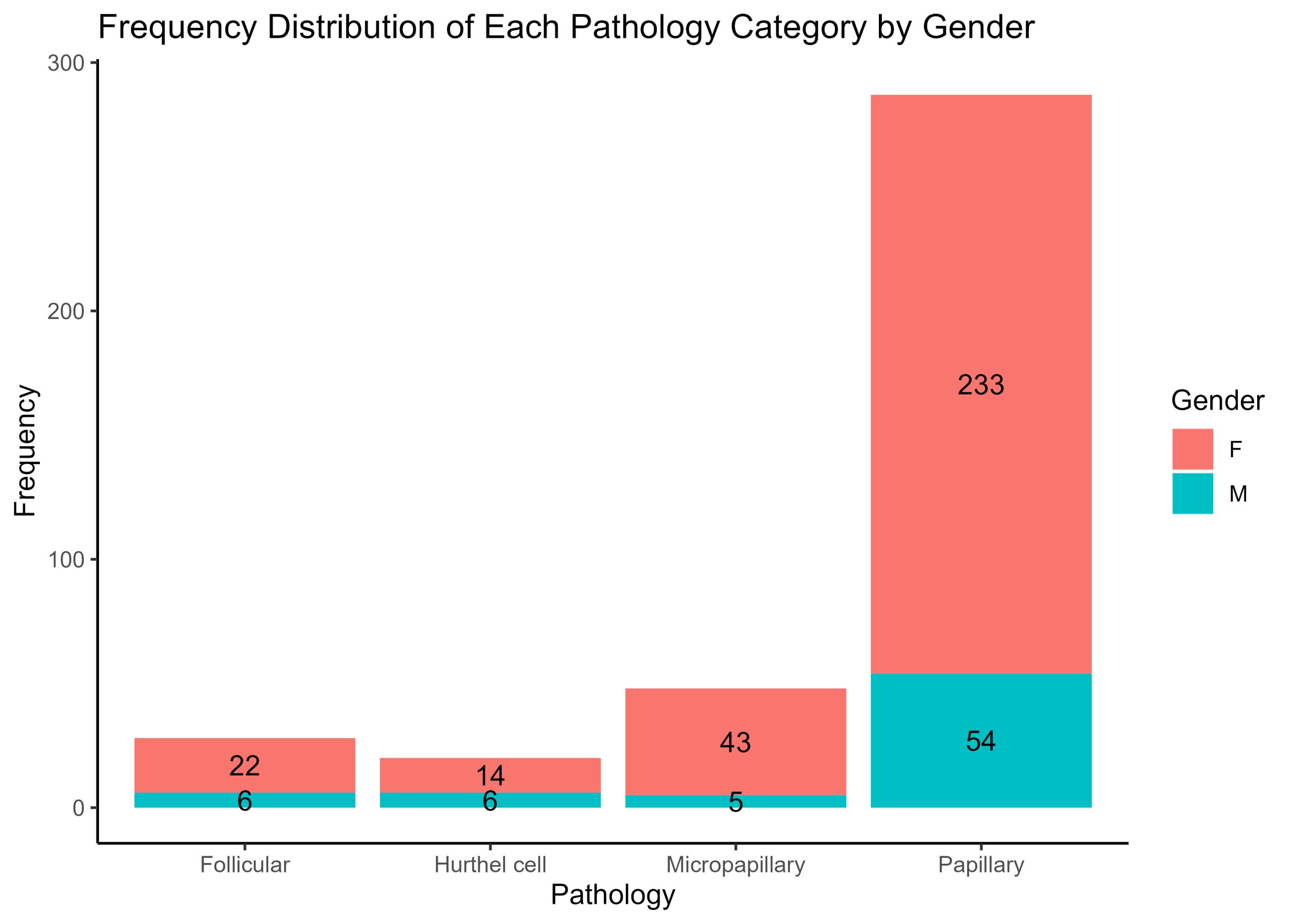
Les histogrammes de fréquence sont un moyen utile de visualiser les nombres et les proportions, mais supposons que vous souhaitiez voir la proportion d’un ensemble de conditions diagnostiques dans une série de pathologies cancéreuses. Pour chaque patient, l’examen physique de la glande thyroïde a été classé dans l’une des cinq catégories suivantes : goitre diffus, goitre multinodulaire, normal, goitre nodulaire unique gauche et goitre nodulaire unique droit.
Il existe quatre pathologies distinctes (comme vous l’avez appris dans l’exercice précédent). Supposons que vous exploitiez ces données et que vous souhaitez connaître les proportions de chaque catégorie de diagnostic physique pour chacune des pathologies. Oui, vous pouvez utiliser un histogramme de fréquence comme développé précédemment, mais vous pouvez également utiliser un diagramme circulaire pour rendre les proportions des catégories de diagnostic physique facilement visibles.
Préparez une série de 4 diagrammes circulaires – un diagramme pour chaque pathologie et, dans chaque diagramme, indiquez la proportion de cas pour chaque catégorie d’examen physique.
#create a custom colour palette :
colour.palette <- c("maroon3", "mediumslateblue", "olivedrab3", "cadetblue2", "darkgoldenrod2" )
# Group by Pathology and Physical.Examination, and count the number of occurrences
pathology_exam_freq <- thyroid.data %>%
group_by(Pathology, Physical.Examination) %>%
summarise(Frequency = n())
# Calculate the total number of each Pathology
total_pathology <- pathology_exam_freq %>%
group_by(Pathology) %>%
summarise(Total = sum(Frequency))
# Join the two dataframes together
pathology_exam_freq <- left_join(pathology_exam_freq, total_pathology, by = "Pathology")
# Calculate the proportion
pathology_exam_freq <- pathology_exam_freq %>%
mutate(Proportion = Frequency / Total)
# Create a pie chart for each Pathology - to see the distribution of physical examination values
Diagnosis.by.Pathology <- pathology_exam_freq %>%
ggplot(aes(x = "", y = Proportion, fill = Physical.Examination)) +
geom_bar(width = 1, stat = "identity") + # fill each bar for a physical examination category
geom_text(aes(label = Frequency), position = position_stack(vjust = 0.5)) +
coord_polar("y", start = 0) + # create a circular histogram- pie chart
facet_wrap(~Pathology) + # this generates a series of 4 plots for each pathology
theme_void() + # aesthetics
theme(legend.position = "right") +
scale_fill_manual(values = colour.palette)+ # fill each bar with a specific colour from palette
labs(fill = "Physical Examination", title = "Proportion of Cases in Each Physical Examination Category by Pathology")
print (Diagnosis.by.Pathology)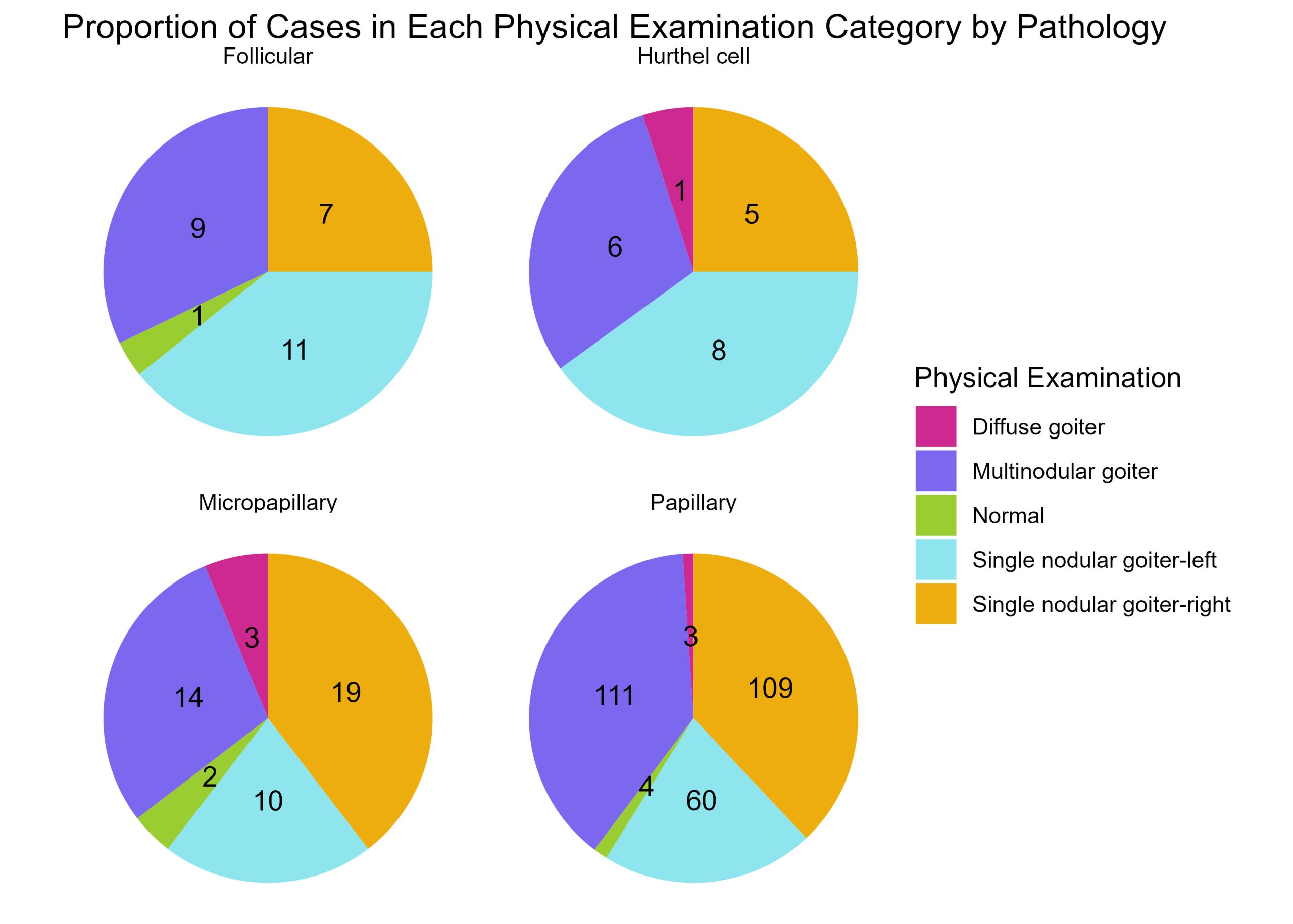
Il s’agit ci-dessus d’un bon moyen de montrer combien de caractéristiques d’examen physique sont présentes dans chaque pathologie cancéreuse. Maintenant, comme vous l’avez fait pour l’histogramme de fréquence ci-dessus, séparez ces données pour montrer les proportions des catégories d’examen physique dans chaque pathologie cancéreuse, par sexe. Cette fois, vous devez créer deux séries de 4 graphiques. Une série pour les hommes et une autre pour les femmes. Chaque graphique montre la proportion de catégories d’examens physiques pour une pathologie donnée.
#create a custom colour palette :
colour.palette <- c("maroon3", "mediumslateblue", "olivedrab3", "cadetblue2", "darkgoldenrod2" )
# Group by Gender, Pathology and Physical.Examination, and count the number of occurrences
gender_pathology_exam_freq <- thyroid.data %>%
group_by(Gender, Pathology, Physical.Examination) %>%
summarise(Frequency = n())
# Calculate the total number of each Gender and Pathology
total_gender_pathology <- gender_pathology_exam_freq %>%
group_by(Gender, Pathology) %>%
summarise(Total = sum(Frequency))
# Join the two dataframes together
gender_pathology_exam_freq <- left_join(gender_pathology_exam_freq, total_gender_pathology, by = c("Gender", "Pathology"))
# Calculate the proportion
gender_pathology_exam_freq <- gender_pathology_exam_freq %>%
mutate(Proportion = Frequency / Total)
# Create a pie chart for each Gender and Pathology
Diagnosis.by.Pathology.by.Gender<- gender_pathology_exam_freq %>%
ggplot(aes(x = "", y = Proportion, fill = Physical.Examination)) +
geom_bar(width = 1, stat = "identity") +
geom_text(aes(label = Frequency), position = position_stack(vjust = 0.5)) +
coord_polar("y", start = 0) +
facet_grid(Gender ~ Pathology) + # create a grid of plots - gender = column, pathologies = rows
theme_void() +
theme(legend.position = "top",
plot.title = element_text(hjust = 0.5)) +
scale_fill_manual(values = colour.palette)+
labs(fill = "Physical Examination", title = "Proportion of Cases for Each Physical Examination Category by Pathology and Gender")
print (Diagnosis.by.Pathology.by.Gender)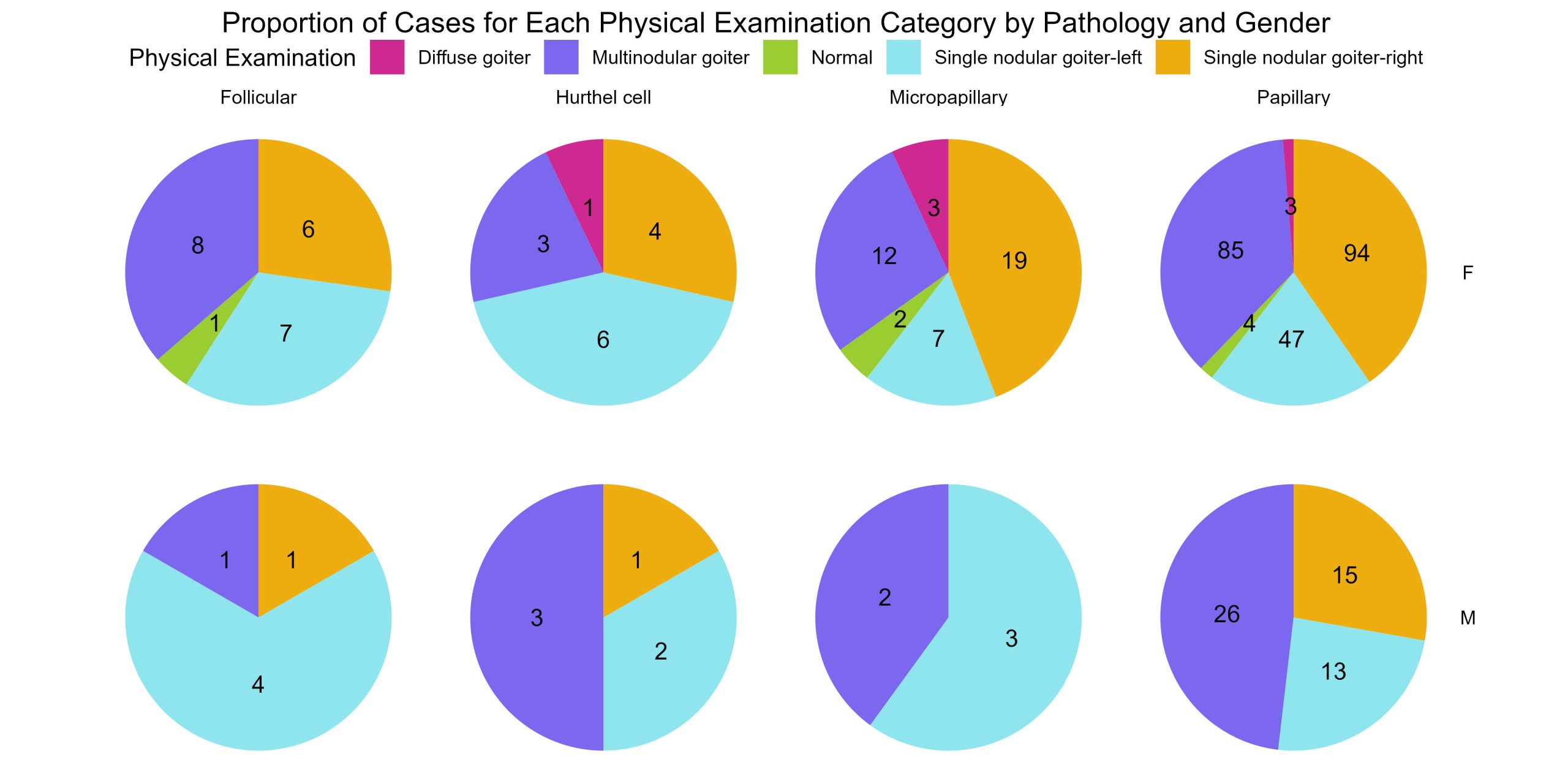
La grammaire de manipulation des données fournie par les progiciels de base de tidyverse constitue un moyen essentiel de regrouper et d’organiser vos données afin de visualiser les tendances, les effectifs et les proportions plus simplement, au moyen de visualisations convaincantes et succinctes.
Un excellent exemple est la création d’une série de diagrammes en boîte. La série de 8 diagrammes circulaires que vous venez de générer dans le dernier exercice montre les proportions des catégories d’examen physique pour chaque pathologie et pour chaque sexe. Mais tous les patients de cet ensemble de données n’ont pas le même âge. Il serait important de connaître également les données démographiques relatives à l’âge. Créez une série de diagrammes en boîte montrant l’âge par sexe pour chaque catégorie d’examen physique pour chaque pathologie cancéreuse. Il s’agit d’une série de 20 diagrammes en boîte.
Cette fois, nous devons utiliser des diagrammes en boîte plutôt que des diagrammes circulaires ou des histogrammes de fréquence, puisque nous voulons montrer l’éventail des âges par sexe pour chaque groupe de catégories.
# Create boxplots of Age by Gender for each Physical.Examination for each Pathology
thyroid.age.boxplots <- thyroid.data %>%
ggplot(aes(x = Gender, y = Age, fill = Gender)) +
geom_boxplot() +
facet_grid(Pathology ~ Physical.Examination) + # produces a grid of plots - each row is a pathology, and each column is a physical examiantion category with boxplots of age by gender
theme(axis.text.x = element_text(angle = 45, hjust = 1)) +
labs(x = "Gender", y = "Age", fill = "Gender", title = "Boxplots of Age by Gender for Each Physical Examination Category by Pathology")
print (thyroid.age.boxplots)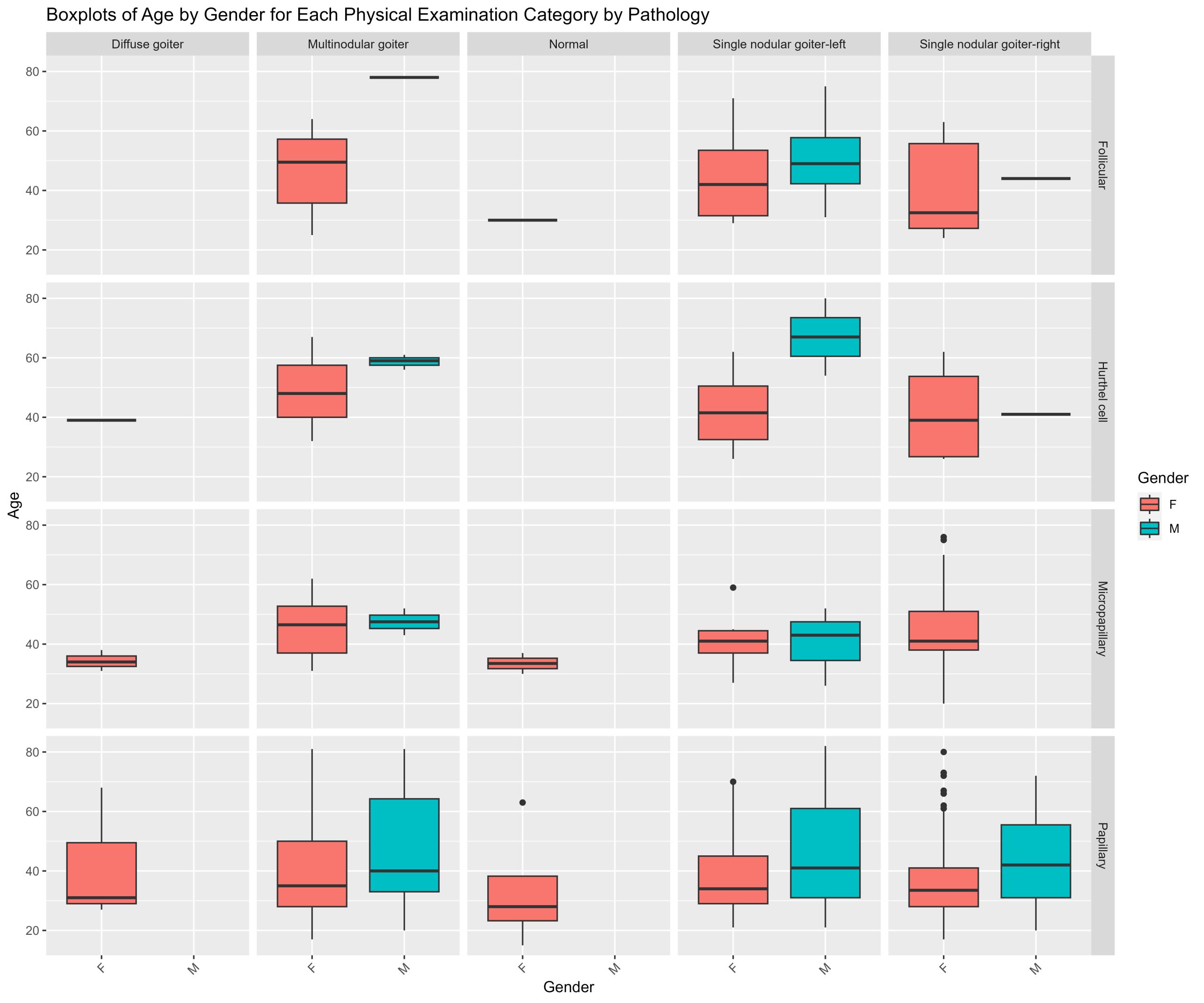
Bien que vous puissiez préparer une série d’effectifs, de proportions ou de diagrammes en boîte pour diverses combinaisons de caractéristiques imbriquées les unes dans les autres. Une étape essentielle consiste à comprendre quelles sont vos caractéristiques, ce que signifient les informations catégorielles contenues dans chaque caractéristique et quelles proportions de vos données se retrouvent dans chaque caractéristique. Vous pouvez y parvenir en créant des diagrammes circulaires pour chaque caractéristique, à l’exception de l’âge du patient. Vous devriez probablement effectuer cette opération au début avant d’entreprendre votre propre analyse d’un ensemble de données catégorielles, mais ce processus est un peu plus compliqué et nous le réservons donc pour la fin. Le processus implique à la fois une série d’opérations de manipulation et des outils de visualisation.
C’est à partir d’analyses exploratoires telles que les graphiques générés dans cette grille de diagrammes circulaires que le chaînage des informations sur les caractéristiques de la pathologie, du sexe, de l’examen physique et de l’âge a semblé intéressant !
# Exclude the "Age" column
data_without_age <- thyroid.data[ , !(names(thyroid.data) %in% "Age")]
# Initialize an empty list to store the plots
plot_list <- list()
## --------------------------------------------- ##
###### loop through columns - get proportions #####
###### & Generate the pie charts each column #####
## --------------------------------------------- ##
for (column_name in names(data_without_age)) {
# Calculate proportions
proportions <- data_without_age %>%
group_by(.data[[column_name]]) %>% # group by common features.
summarise(n = n()) %>% # produce summary statistics
mutate(prop = n / sum(n)) # mutate produces a column with proportions in one step
# Create pie chart
pie_chart <- ggplot(proportions, aes(x = "", y = prop, fill = .data[[column_name]])) +
geom_bar(width = 1, stat = "identity") +
coord_polar("y", start = 0) +
labs(title = paste("Pie Chart for", column_name), x = NULL, y = NULL, fill = column_name) +
theme(plot.margin = margin (1,1,1,1, "cm"))+ # common margin to each plot
theme_void() #aesthetics - blank backgrounds
# Add the pie chart to the list
plot_list[[column_name]] <- pie_chart
}
# Arrange the plots into a grid
plotgrid <- grid.arrange(grobs = plot_list, ncol = 4, returnGrob= TRUE)
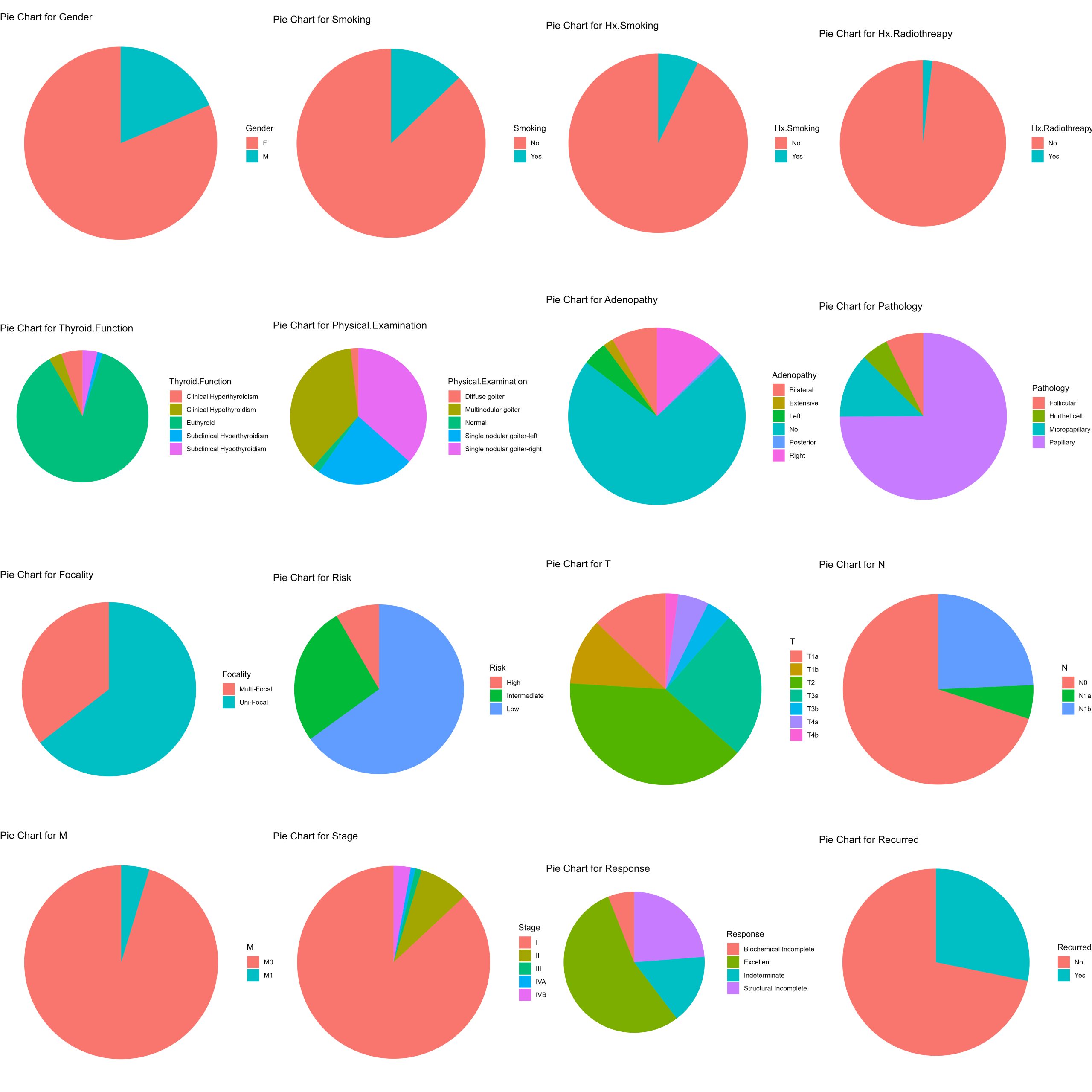
Pour télécharger, cliquez avec le bouton droit de la souris et appuyez sur “Enregistrer le fichier sous” ou “Télécharger le fichier lié”.
Vous êtes pathologiste et vous avez mesuré 569 noyaux de cellules à partir de prélèvements à l’aiguille de masses de tissu mammaire. Les échantillons proviennent de masses bénignes (B) ou malignes (M). Vous souhaitez effectuer une analyse de la forme et de la taille des cellules entre les cellules bénignes et malignes afin de mieux comprendre les différences qui existent entre elles. Vous aimeriez également explorer l’utilisation de l’apprentissage automatique pour voir dans quelle mesure de simples algorithmes de regroupement peuvent identifier les cellules bénignes des cellules malignes en se basant UNIQUEMENT sur leurs caractéristiques de taille et de forme. Utilisation de l’ensemble de données sur le cancer du sein du Wisconsin
—- Texte tiré de Kaggle ——-
Les données sur le cancer du sein comprennent 569 exemples de biopsies cancéreuses, chacune comportant 32 caractéristiques. Une caractéristique est un numéro d’identification, une autre est le diagnostic du cancer et 30 sont des mesures de laboratoire à valeur numérique. Le diagnostic est codé “M” pour malin ou “B” pour bénin.
Les 30 autres mesures numériques comprennent la moyenne, l’erreur standard et la valeur la plus mauvaise (c’est-à-dire la plus grande) pour 10 caractéristiques différentes des noyaux cellulaires numérisés, qui sont les suivantes:-
Rayon, Texture ,Périmètre, Surface, Lisse Compacité, Concavité, Concave Points, Symétrie ,Dimension fractale. Les données sont disponisbles du : https://archive.ics.uci.edu/dataset/17/breast+cancer+wisconsin+diagnostic
Pour en savoir plus sur l’ensemble de données du Wisconsin sur le cancer du sein, et plus particulièrement sur la manière dont chacune des caractéristiques de cet ensemble de données a été calculée, veuillez consulter :
Street, W.N., Wolberg, W.H., & Mangasarian, O.L. (1993). Nuclear feature extraction for breast tumor diagnosis. Electronic imaging.
Installez et chargez les progiciels suivants dans votre environnement de RStudio.
library(dabestr) # estimation statistics
library(ggplot2) # plotting and data visualisation
library(pheatmap) # generating a heatmap
library(tidyverse) # data handling
library(dplyr) # data handling
library(stats) # basic statistics
library(RColorBrewer) # colour palettes and plot aesthetic controls
library(Rtsne) # for performing T-distributed stochastic neighbour embedding (tsne)
Téléchargez les données à partir du UCI Machine Learning Repository. Charger ensuite le fichier csv des mesures des cellules dans votre environnement de RStudio.
BreastCancer.Data <- read.csv("WisconsinBreastCancerData.csv")
BreastCancer.Data$X <- NULL
print (head(BreastCancer.Data))L’ensemble de la base de données BreastCancer.Data est structuré de telle sorte que chaque ligne correspond à une cellule et chaque colonne à un paramètre. Toutefois, certaines colonnes ne sont pas des caractéristiques (descriptions quantitatives des cellules). Lorsqu’une colonne n’est pas une caractéristique, il s’agit d’une étiquette. Les étiquettes sont des moyens d’identifier ou de marquer des cellules spécifiques une fois que nous avons compris comment elles sont caractérisées par leurs caractéristiques.
Avant de pouvoir explorer l’ensemble de données, nous devons séparer les étiquettes des caractéristiques. Deux colonnes du cadre de données étiquettent les cellules – id -> le numéro d’identification unique attribué à une cellule – diagnostic -> si la cellule provient d’un échantillon bénin (B) ou malin (M)).
Les colonnes restantes sont des caractéristiques qui servent de descriptions quantitatives de la taille et de la forme des cellules.
## ---------------------------------------- ##
##### Setting features apart from labels #####
## ---------------------------------------- ##
# labels dataframe - contains the unique identifier and the diagnosis)
Diagnostic.Labels <- select(BreastCancer.Data, id, diagnosis)
# features dataframe - all the columns that are not identifiers are the measured features that characterise the tissue mass - specifically the characterizing the nuclei present.
feature.columns <- setdiff (colnames(BreastCancer.Data), colnames(Diagnostic.Labels))
Diagnostic.Features <- BreastCancer.Data[, feature.columns]
# create a z-scored version of the features
Diagnostic.Features.Scored <- scale(Diagnostic.Features)
# print (head(Diagnostic.Features.Scored))
view(Diagnostic.Features.Scored)
print (colnames(Diagnostic.Features.Scored)Tsne ou le T-distributed Stochastic Neighbour Embedding est une technique utilisée pour visualiser des données de haute dimension en 2 dimensions. Qualifiée de méthode de réduction de la dimensionnalité, elle nous permet d’explorer les données une caractéristique à la fois. Dans cet ensemble de données sur le cancer du sein, 32 mesures décrivent la taille, la forme et la texture des masses dans le tissu mammaire, qui sont ensuite considérées comme bénignes (B) ou malignes (M).
Pour plus d’informations sur T-sne, veuillez consulter : Van der Maaten, L., Hinton, G. Visualizing Data using T-sne. Journal of Machine Learning Research 9 (2008) 2579-2605
Utilisons tsne pour visualiser la répartition de ces caractéristiques dans l’ensemble des données.
N.B. J’ai exécuté cette boucle for de combinaisons de semences par perplexité car il est important de tester ces paramètres lorsque l’on travaille avec T-sne. La perplexité contrôle la part des éléments de la structure de données locale par rapport aux éléments de la structure de données globale qui contribuent à la visualisation finale lorsque les données passent par la réduction de la dimensionnalité. Les variations de perplexité pour la même graine aléatoire peuvent avoir des effets très importants sur la visualisation finale, même si les données ne changent pas.
# Define your perplexities and seeds
perplexities <- c(10, 15, 20, 25, 30)
seeds <- c(123, 456, 789, 246, 135 )
# Create an empty dataframe to store the t-SNE components
tsne_data <- data.frame()
# Iterate over each combination of perplexity and seed
for (i in 1:length(perplexities)) {
for (j in 1:length(seeds)) {
# Perform t-SNE with the current perplexity and seed
tsne_model <- Rtsne(Diagnostic.Features.Scored, perplexity = perplexities[i], seed = seeds[j])
# Create a dataframe for the t-SNE components
tsne_temp <- data.frame(
tSNE1 = tsne_model$Y[, 1],
tSNE2 = tsne_model$Y[, 2],
Perplexity = perplexities[i],
Seed = seeds[j],
Diagnosis = Diagnostic.Labels$diagnosis
)
# Append the data to the main dataframe
tsne_data <- rbind(tsne_data, tsne_temp)
}
}
# Create the plot
tsne.stampcollection <- ggplot(tsne_data, aes(x = tSNE1, y = tSNE2, colour = Diagnosis)) +
geom_point() +
facet_wrap(Perplexity ~ Seed, scales = "free") +
theme_bw()
Utilisez les paramètres suivants dans votre tsne initial : – seed <- 789 – perplexité <- 30
Construisez une carte T-sne de la base de données Diagnostic.Features. Tracez la carte T-sne résultante à l’aide de ggplot en veillant à colorer les points en fonction de leur étiquette de diagnostic. Que remarquez-vous sur la carte T-sne lorsqu’elle est annotée par diagnostic ?
En guise d’exercice, variez la perplexité pour la graine de 789, en essayant d’aller de 10 à 50 par sauts de 10. Que remarquez-vous sur la carte T-sne lorsque vous faites varier la perplexité ? Selon vous, que contrôle le paramètre de perplexité dans l’algorithme T-sne ?
# Set your perplexity and seed
set.seed (789)
perplexity <- 30
seed <- 789
# Perform t-SNE with the specified perplexity and seed
tsne_model <- Rtsne(Diagnostic.Features.Scored, perplexity = perplexity, seed = seed)
# Create a dataframe for the t-SNE components
tsne_data <- data.frame(
tSNE1 = tsne_model$Y[, 1],
tSNE2 = tsne_model$Y[, 2],
Diagnosis = Diagnostic.Labels$diagnosis # Add the diagnosis column
)
# Load ggplot2
library(ggplot2)
# Create the plot
tsne.by.diagnosis <- ggplot(tsne_data, aes(x = tSNE1, y = tSNE2, colour = Diagnosis)) +
geom_point() +
labs( x = "T-SNE Component 1", y= "T-SNE Component 2")
theme_bw()
# Print the plot
print(tsne.by.diagnosis)
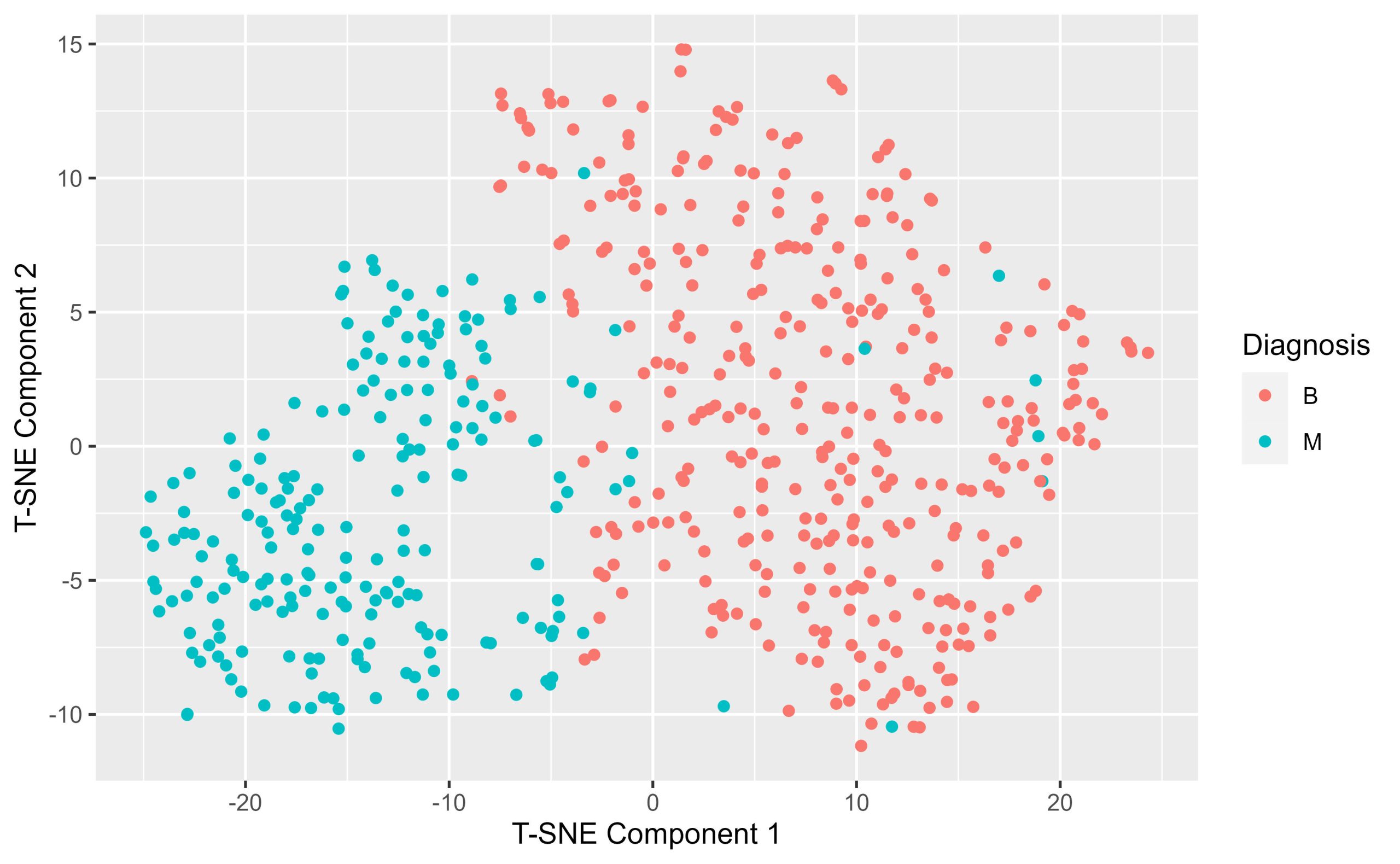
Et s’il existait un moyen d’identifier facilement les cellules comme étant bénignes ou malignes en fonction de leurs paramètres de taille et de forme ? Les algorithmes de regroupement sont un exemple d’approche fondée sur les données pour regrouper vos données sur la base des modèles présents dans les caractéristiques. Bien sûr, les données contiennent des étiquettes, mais que se passerait-il si vous faisiez des regroupements sur les valeurs des caractéristiques, les mesures, sans fournir d’informations sur le diagnostic des cellules ? Sélectionnez 2 grappes – nous voulons voir si le regroupement hiérarchique permet de distinguer les cellules bénignes des cellules malignes en se basant uniquement sur les informations relatives à leur forme et à leur taille.
Les étapes du regroupement hiérarchique sont les suivantes :
## ----------------------------------------------------- ##
#### dissimilarity matrix and hierarchical clustering #####
## ----------------------------------------------------- ##
# set the number of clusters
num.clusters <- 2
# construct a pairwise dissimilarity matrix using euclidean distances
dissimilarity.matrix <- dist(Diagnostic.Features.Scored, method = "euclidean")
# hierarchical clustering with Wthe ward.D2 algorithm
h.clusters <- hclust(dissimilarity.matrix, method = "ward.D2")
# cut the dendrogram into k clusters
clusters <- cutree(h.clusters, k = num.clusters)
## --------------------------------------------------- ##
##### Preparing Dataframe for Downstream Statistics #####
## --------------------------------------------------- ##
# create a dataframe of identifiers and z-scored features
All.Samples.zscored <- cbind(Diagnostic.Labels,
Diagnostic.Features.Scored)
# append the clusters to the dataframe
All.Samples.zscored$hclust_clusters <- clusters
# view(Malignant.Samples.zscored) # inspection step
##--------------------------------------- ##
##### Annotating the HClust Dendrogram #####
##--------------------------------------- ##
# create an annotation dataframe
annotation.df <- data.frame(Cluster = as.factor(clusters))
rownames(annotation.df) <- rownames(Diagnostic.Features)
# apply a colour palette to the annotations on the dendrogram
# colour palette for the k clusters
k.cluster.colourpalette <- c("olivedrab2", "maroon3")
# colour mapping
colourmapping <- setNames(k.cluster.colourpalette, levels (annotation.df$Cluster))
# make a list of annotation colours
annotation.colours = list(Cluster = k.cluster.colourpalette)
# match the names of the annotation colours to the cluster levels ( 1-8)
names(annotation.colours$Cluster) <- levels(annotation.df$Cluster)
## ----------------------------------------- ##
##### visualising clustering in a heatmap #####
## ----------------------------------------- ##
# set a colour palette
# diverging - spectral
div.spectral.red.blue <- c("#4a100e", "#731331", "#a52747", "#c65154", "#e47961", "#f0a882", "#fad4ac", "#ffffff",
"#bce2cf", "#89c0c4", "#5793b9", "#397aa8", "#1c5796", "#163771", "#10194d" )
div.spectral.blue.red <- rev(div.spectral.red.blue)
# interpolate the colours for continuous scales
continuous.spectral.redblue <- colorRampPalette(div.spectral.red.blue) (256)
continuous.spectral.bluered <- colorRampPalette(div.spectral.blue.red)(256)
# set the breaks in the colour scale
palette.breaks <- seq(from= 0, to = 8, length.out = length (continuous.spectral.redblue) + 1)
# generate the heatmap
hclust.dissimilarity.heatmap <- pheatmap(dissimilarity.matrix,
cluster_rows = h.clusters,
cluster_cols = h.clusters,
annotation_row = annotation.df,
# annotation_col = annotation.df,
annotation_colors = annotation.colours,
color = continuous.spectral.redblue,
breaks = palette.breaks)
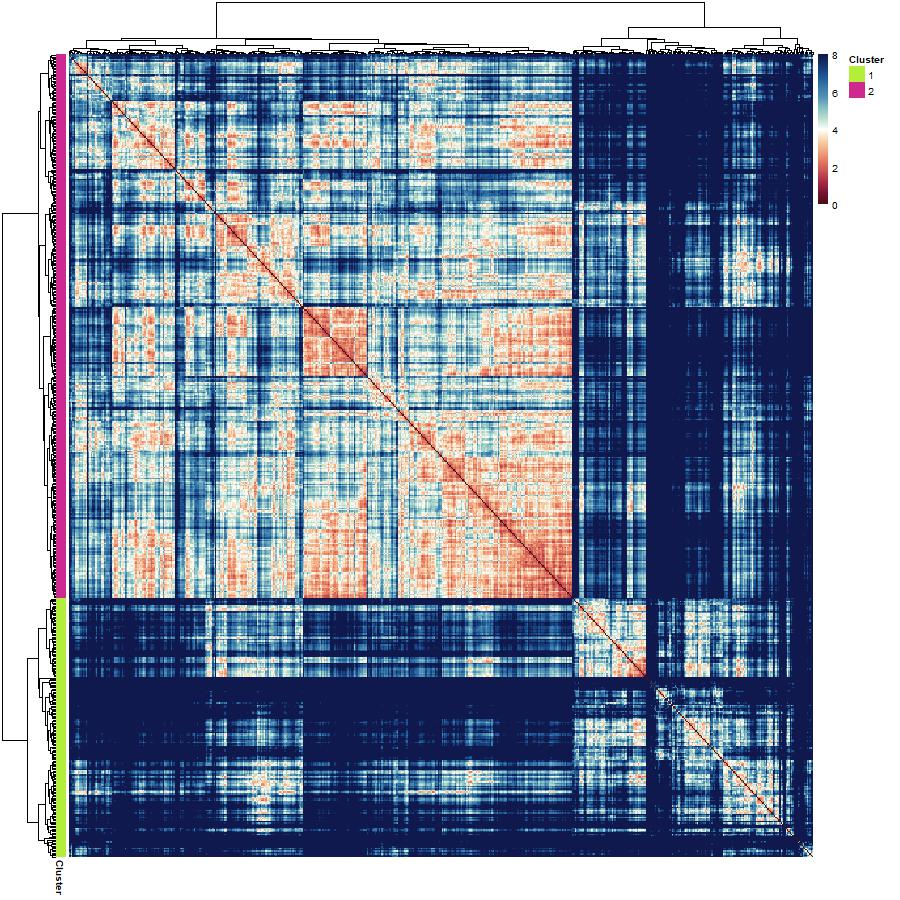
Vous venez de produire un résultat de regroupement hiérarchique. Vous pouvez visualiser le regroupement à l’aide d’une carte thermique et d’un dendrogramme annoté, mais cela ne vous permet pas de savoir quelles cellules ont été reléguées dans quel regroupement. Vous pouvez également produire un diagramme à barres de proportions empilées qui vous indique la proportion de cellules bénignes et malignes dans un groupe.
Préparez un cadre de données de proportions – regroupez les données par groupe et par diagnostic et calculez les pourcentages.
préparez un diagramme à barres de proportions empilées à l’aide de ggplot et de l’élément geom_bar. D’après les résultats du regroupement, dans quelle mesure le regroupement hiérarchique a-t-il permis de distinguer les cellules bénignes des cellules malignes ?
– Question de l’étudiant – Parmi les caractéristiques de votre cadre de données, il existe des modèles qui permettent de distinguer les cellules bénignes des cellules malignes. Vous souhaitez évaluer la différence entre les cellules bénignes et les cellules malignes.
library(dplyr)
# Calculate proportions of benign and malignant cells by cluster
# you can use the pipe operator to nest a series of operations to be performed to the dataframe of origin
All.Samples.zscored.grouped <- All.Samples.zscored %>%
group_by(hclust_clusters, diagnosis) %>%
summarise(n = n()) %>%
mutate(freq = n / sum(n))
view (All.Samples.zscored.grouped)
# Prepare a stacked proportion barplot
Hclust.barplot <- ggplot(All.Samples.zscored.grouped, aes(fill=diagnosis, y=freq, x=hclust_clusters)) +
geom_bar(position="fill", stat="identity") +
theme_minimal() +
labs(x="Cluster", y="Proportion", fill="Diagnosis") +
scale_x_continuous(breaks = c(1,2))+
theme(axis.text.x = element_text(angle = 90, hjust = 1))
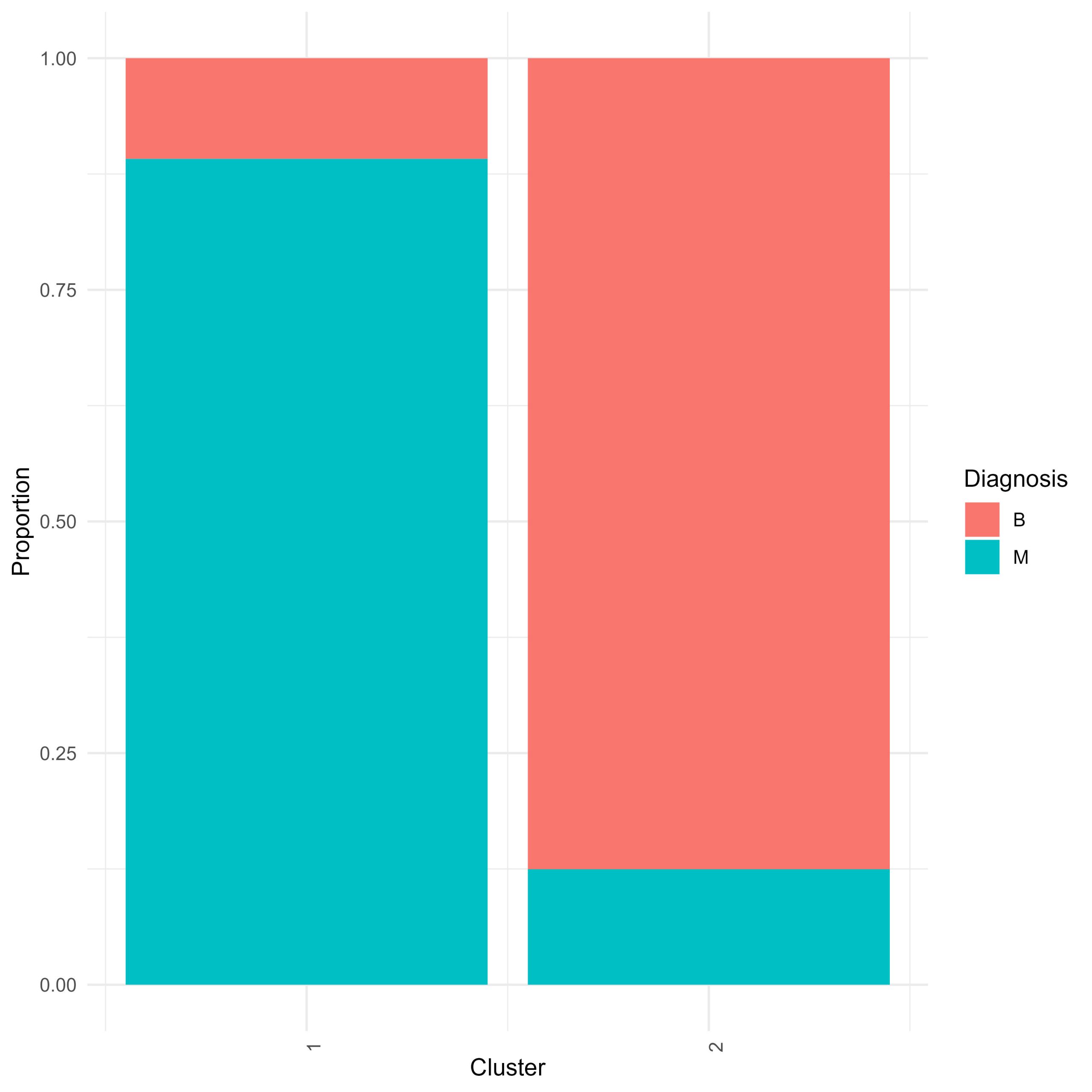
Les statistiques d’estimation constituent un cadre alternatif pour l’analyse statistique qui ne dépend pas des valeurs p ou des tests de signification. Au lieu de cela, elles montrent les données, les distributions et leurs différences médianes non appariées, ainsi que les intervalles de confiance à 95 % amorcées. Ce cadre vous permet de voir vos données et d’évaluer la différence ou l’absence de différence sans test de signification. Il s’agit d’un cadre puissant qui rend l’inférence statistique visuellement accessible et franchement belle !
Les statistiques d’estimation précédentes ont été appliquées aux cellules classées par étiquette de diagnostic – pour évaluer les différences de caractéristiques entre les cellules bénignes et malignes. Cette fois, répétez le même cadre de statistiques d’estimation et examinez les mêmes caractéristiques, mais appliquez les statistiques d’estimation aux grappes à la place. Comment les graphiques d’estimation par grappe se comparent-ils aux graphiques d’estimation par étiquette diagnostique ?
Pour plus d’informations sur les statistiques d’estimation, veuillez consulter : Ho et al. 2019. publié dans Nature Methods
Ho, J., Tumkaya, T., Aryal, S. et al. Moving beyond P values : data analysis with estimation graphics. Nat Methods 16, 565-566 (2019). https://doi.org/10.1038/s41592-019-0470-3
# names of clusters
# cluster_names <- c("B", "M") # performing estimation stats by diagnostic label
cluster_names <- c("1", "2") # if performing estimation stats by hclust defined clusters
feature.of.interest <- "fractal_dimension_mean"
data1 <- All.Samples.zscored %>%
# select(variable = "diagnosis", value = feature.of.interest) # estimation on diagnostic labels
select (variable = "hclust_clusters", value = feature.of.interest) # estimation on the hclust clusters
estimation.stats.data <- data1
# Specify your reference group
# reference_group <- "B" # estimation by diagnostic label ( B = Benign, M = Malignant)
reference_group <- "1" # estimation by hclust cluster
# set the control group
control = reference_group
# set the comparison groups
comparisons = setdiff(cluster_names, control)
# Set the column names
colnames(estimation.stats.data)[2] = "Z-Scored Mean Nuclear Fractal Dimension"
# Prepare data for estimations statistics processing
two.group.unpaired =
estimation.stats.data %>%
dabest(variable,`Z-Scored Mean Nuclear Fractal Dimension`,
idx = c(control, comparisons),
paired = FALSE) %>%
median_diff(reps = 10000)
# Set the color parameters
# colour palette corresponds to diagnostic labels
# colours = c("coral2", "turquoise3" )
# colour palette corresponds to hierarchically defined clusters
colours = c("maroon3", "olivedrab2")
colour.swarm.plot = c(colours[which(cluster_names == control)],
setdiff(colours,
colours[which(cluster_names == control)]))
swarm.plot <- plot(two.group.unpaired,
palette = colour.swarm.plot,
# tick.fontsize = 20,
# axes.title.fontsize = 25,
rawplot.type = "swarmplot",
rawplot.ylabel = "Z-Scored Mean Nuclear Fractal Dimension")+
ggtitle(paste("Reference: cluster ", control))+
theme(title = element_text(face = "bold"),
plot.title = element_text(hjust = 0.5, vjust = 10, size = 20,
margin = margin(t = 80, b = -35)))
print(swarm.plot)
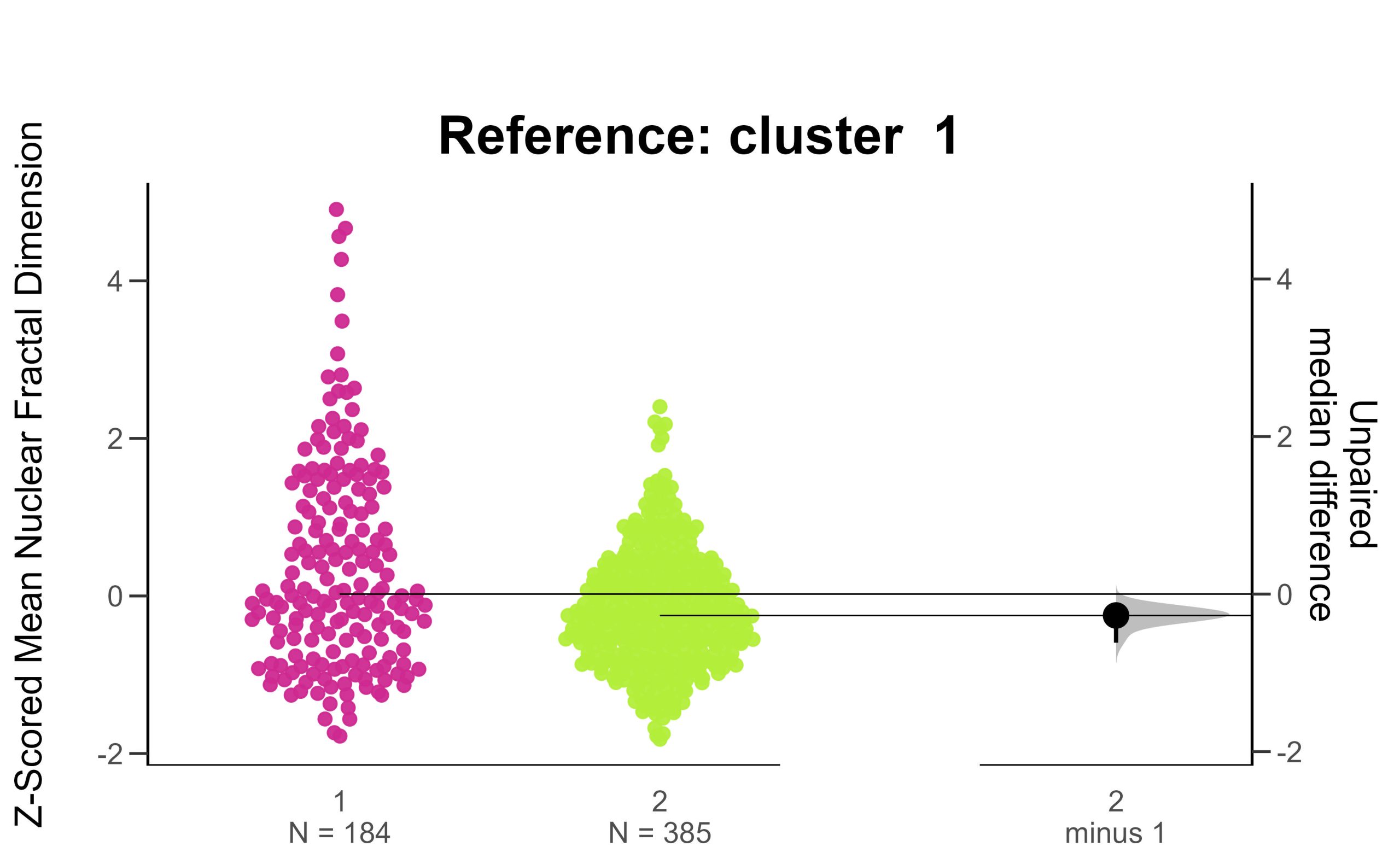
Une autre façon d’évaluer l’efficacité de l’affectation des grappes en fonction de l’étiquette de diagnostic consiste à annoter le graphique T-SNE que vous avez construit précédemment, mais cette fois-ci, au lieu de colorer les points en fonction de leur étiquette de diagnostic connue, vous pouvez les annoter en fonction de leurs grappes définies de façon hiérarchique.
Utilisez la même perplexité et la même graine aléatoire que précédemment. De cette façon, vous pouvez comparer la façon dont les grappes de grappes sont représentées dans l’espace à haute dimension et la façon dont les étiquettes de diagnostic sont représentées dans le même espace. Lorsque vous comparez les graphiques t-SNE annotés par diagnostic et par grappe hiérarchique, que remarquez-vous ? Quelles sont les similitudes et les différences qui vous semblent évidentes ?
## --------------------------------------------------- ##
##### Repeat T-SNE code but plot coloured by hclust #####
## --------------------------------------------------- ##
# Set your perplexity and seed
set.seed (789)
perplexity <- 30
seed <- 789
# Perform t-SNE with the specified perplexity and seed
tsne_model <- Rtsne(Diagnostic.Features.Scored, perplexity = perplexity, seed = seed)
# Create a dataframe for the t-SNE components
tsne_data <- data.frame(
tSNE1 = tsne_model$Y[, 1],
tSNE2 = tsne_model$Y[, 2],
hclust_cluster = as.factor(All.Samples.zscored$hclust_clusters) # Add the Hierarchical Cluster Assignment - convert to factor to make the scale discrete
)
view( tsne_data)
# Load ggplot2
library(ggplot2)
# specify the colour palette :
hclust.colours <- c("maroon3", "olivedrab2")
# Create the plot
tsne.by.hcluster <- ggplot(tsne_data, aes(x = tSNE1, y = tSNE2, colour = hclust_cluster)) +
geom_point() +
labs( x = "T-SNE Component 1", y= "T-SNE Component 2") +
theme_bw() +
scale_color_manual(values = hclust.colours)
# Print the plot
print(tsne.by.hcluster)
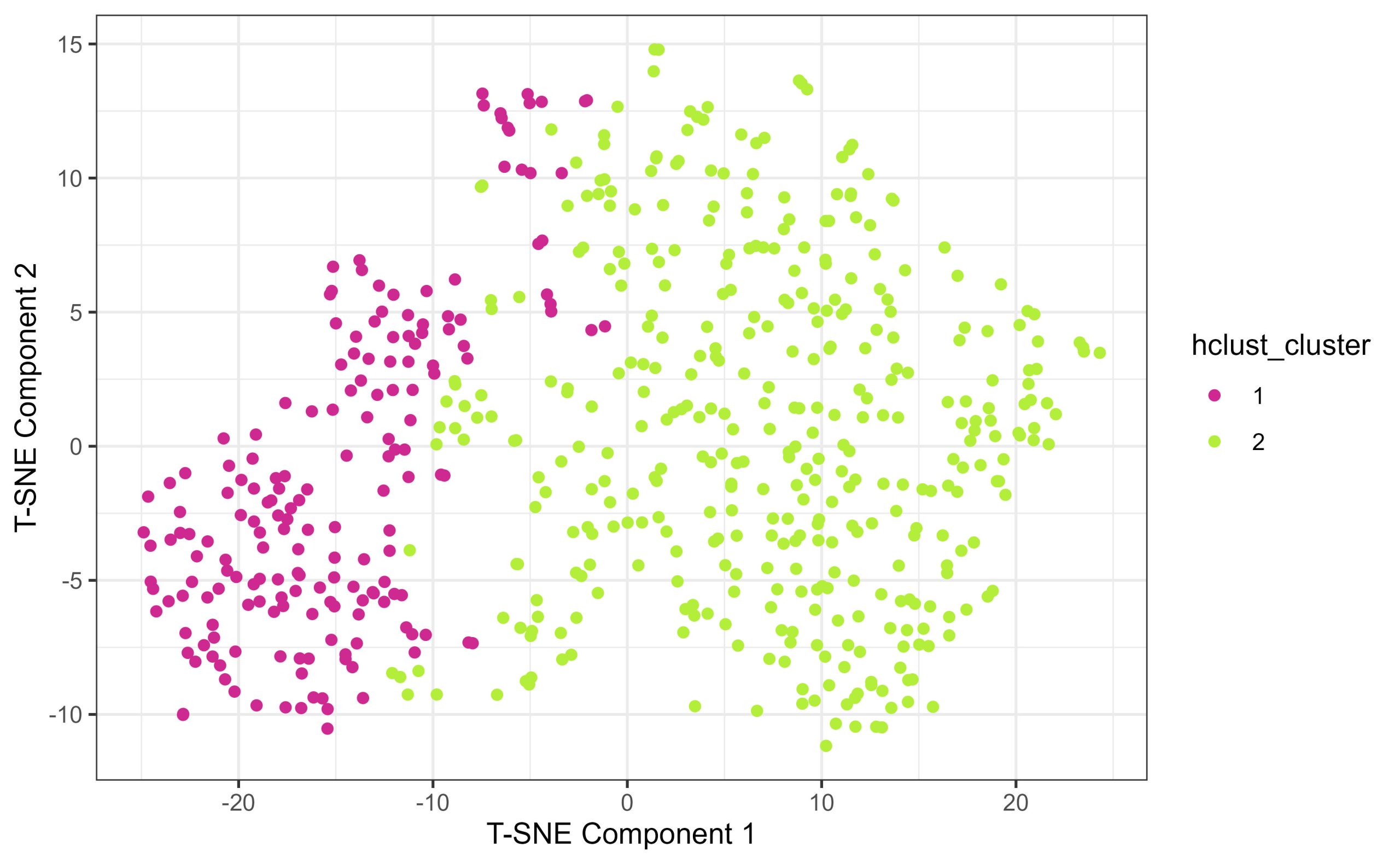
(réflexion des élèves – peut donner lieu à une discussion sur les algorithmes de regroupement et sur les raisons pour lesquelles il est important de vérifier et de valider les résultats des regroupements)
Vous avez comparé les véritables étiquettes diagnostiques des cellules cancéreuses du sein – bénignes et malignes – à des clusters hiérarchiques construits uniquement à partir de caractéristiques de taille et de forme. Compte tenu de l’efficacité avec laquelle l’algorithme de regroupement a séparé les cellules bénignes et malignes, réfléchissez à l’utilité de cette approche si vous ne saviez pas a priori que les cellules étaient classées dans les catégories de diagnostic bénigne et maligne. Après les avoir regroupées en deux groupes et avoir comparé leurs statistiques, que devriez-vous faire pour confirmer que les cellules d’un groupe sont malignes et que les autres sont bénignes ?
III
Vous êtes un biologiste évolutionniste étudiant le conflit sexuel et l’effet de la fréquence des accouplements sur la condition physique des femelles tout au long de leur vie. Votre système d’étude est le tristement célèbre punaise de lit Climex lectularis. Les punaises de lit vivent en agrégations mixtes où les femelles sont sujettes à un harcèlement reproductif fréquent de la part des mâles. En raison de ce harcèlement reproductif, les femelles varient dans leurs taux d’accouplement dans les groupes naturels où certaines femelles s’accouplent relativement rarement, et d’autres beaucoup plus fréquemment. Des taux d’accouplement plus élevés pour les femelles augmentent le nombre de descendants produits par unité de temps, mais peuvent imposer une pénalité de longévité car le processus physique de reproduction est coûteux. Ce compromis pose la question de savoir si la variation du taux d’accouplement entraîne un changement de la condition physique globale tout au long de la vie (nombre de descendants viables produits). Pour répondre à cette question, vous avez soumis les femelles à un traitement de fréquence d’accouplement élevée (High) ou faible (Low). Vous avez compté le nombre total de descendants viables que chaque femelle a produit au cours de sa vie (Hatchlings), ainsi que sa durée de vie totale en jours (Longevity). Vous avez enregistré vos résultats dans le dataframe contenu dans “femalefitness.csv”.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=203#h5p-64
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=203#h5p-65
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=203#h5p-66
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=203#h5p-67
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=203#h5p-68
Pour télécharger, faites un clic droit et appuyez sur “Enregistrer le fichier sous” ou “Télécharger le fichier lié”
Cognitive Ecology Lab, Dr. Reuven Dukas, Département de Psychologie, Neuroscience, & Comportement de l’Université McMaster https://psych.mcmaster.ca/dukas/index.htm
Yan, J. L., & Dukas, R. (2022). The social consequences of sexual conflict in bed bugs: social networks and sexual attraction. Animal Behaviour, 192, 109-117.
Parker, G. A. (2006). Sexual conflict over mating and fertilization: an overview. Philosophical Transactions of the Royal Society B: Biological Sciences, 361(1466), 235-259.
Maklakov, A. A., Bilde, T., & Lubin, Y. (2005). Sexual conflict in the wild: elevated mating rate reduces female lifetime reproductive success. the american naturalist, 165(S5), S38-S45.
Vous êtes un écologiste comportemental intéressé par la territorialité et l’agression chez les grenouilles. La grenouille venimeuse à cuisses brillantes Allobates femoralis dépend de la présence de petites mares d’eau pour sa reproduction. Les mâles de cette espèce se livrent à une compétition territoriale pour sécuriser les zones qui contiennent ces mares d’eau. On ignore cependant à quel moment du développement des grenouilles le comportement territorial émerge. Pour tester cela, vous avez voyagé jusqu’à un site de terrain en Équateur oriental et capturé 50 A. femoralis de divers stades de développement. Vous avez enregistré le sexe de chaque grenouille, mesuré la longueur du museau au cloaque (SVL ; en mm) de chaque grenouille, puis soumis les grenouilles à un test de miroir. Dans le test de miroir, vous avez enregistré si elles exprimaient des comportements agressifs (par exemple, des charges, des morsures ou des luttes) envers leur reflet dans le miroir.
Note : Ce scénario implique une analyse statistique plus avancée connue sous le nom de “Régression logistique”, non couverte ni par les statistiques descriptives ni par les statistiques inférentielles. Le principe général de la régression logistique est de déterminer si une variable prédictive a un effet sur le résultat d’une variable de réponse catégorielle. Dans ce scénario, notre résultat catégoriel est binaire (pas d’agression, 0, versus agression, 1). Cela fait de ce scénario plus spécifiquement une “Régression binomiale”, qui est un sous-ensemble de la régression logistique. Pour une introduction sur la façon de réaliser une régression binomiale en R, voir :
https://bookdown.org/ndphillips/YaRrr/logistic-regression-with-glmfamily-binomial.html
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=205#h5p-70
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=205#h5p-71
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=205#h5p-72
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=205#h5p-73
Pour télécharger, faites un clic droit et appuyez sur “Enregistrer le fichier sous” ou “Télécharger le fichier lié”
Laboratoire d’Écologie Comportementale et Sensorielle, Dr. James B. Barnett, Département de Zoologie, Trinity College Dublin, Irlande
Chaloupka, S., Peignier, M., Stückler, S., Araya-Ajoy, Y., Walsh, P., Ringler, M., & Ringler, E. (2022). Repeatable territorial aggression in a Neotropical poison frog. Frontiers in ecology and evolution, 10, 881387.
Rodríguez, C., Fusani, L., Raboisson, G., Hödl, W., Ringler, E., & Canoine, V. (2022). Androgen responsiveness to simulated territorial intrusions in Allobates femoralis males: evidence supporting the challenge hypothesis in a territorial frog. General and comparative endocrinology, 326, 114046.
Vous êtes un écologiste visuel étudiant la coloration d’avertissement et le mimétisme chez les grenouilles à fléchettes empoisonnées. Votre système d’étude est l’Ameerega bilinguis toxique et l’Allobates zaparo non toxique, une paire d’espèces de grenouilles terrestres sympatriques originaires de l’Amazonie équatorienne. L’Ameerega bilinguis utilise un signal d’avertissement à plusieurs composants, avec un dos rouge, des taches lumineuses jaunes sur les membres et un ventre bleu vif. L’Allobates zaparo a évolué pour imiter cette coloration, mais présente un “mimétisme imparfait” – les propriétés quantitatives exactes des composants de couleur ne sont pas parfaitement assorties. Vous avez collecté 20 individus adultes de chaque espèce sur le terrain et pris des photographies calibrées en couleur de chacune de leurs régions corporelles. Vous avez ensuite utilisé la micaToolbox dans ImageJ pour simuler la vision aviaire et calculer la force du contraste chromatique (c’est-à-dire la teinte) et achromatique (c’est-à-dire la luminosité) de chacun des quatre composants de couleur (Front Spots, Back Spots, Dorsum, Venter) contre un arrière-plan naturel de feuilles mortes, pour chaque espèce. Les valeurs de contraste visuel sont présentées dans l’unité de ‘JND’, ou ‘Just Noticeable Difference’, où des valeurs plus élevées indiquent que la tache de couleur contraste plus fortement avec l’arrière-plan. En d’autres termes, des valeurs plus élevées signifient que le composant du signal est plus visible.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=207#h5p-74
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=207#h5p-75
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=207#h5p-76
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=207#h5p-77
Pour télécharger, faites un clic droit et appuyez sur “Enregistrer le fichier sous” ou “Télécharger le fichier lié”
Laboratoire d’Écologie Comportementale et Sensorielle, Dr. James B. Barnett, Département de Zoologie, Trinity College Dublin, Irlande
McEwen, B.L., Yeager, J.D., Kinley, I., Anderson, H.M., Barnett, J.B.B. (Under Review). Body posture and viewing angle modulate detectability and mimic fidelity in a poison frog system.
Darst, C. R., & Cummings, M. E. (2006). Predator learning favours mimicry of a less-toxic model in poison frogs. Nature, 440(7081), 208-211.
Stevens M, Párraga CA, Cuthill IC, Partridge JC, Troscianko TS. (2007). Using digital photography to study animal coloration. Biol. J. Linn. 90, 211-237
Vous êtes un herpétologiste intéressé par les invasions biologiques dans les habitats urbains. L’anole brun Anolis sagrei est une espèce invasive en Floride du Sud, où il est maintenant en concurrence avec l’anole vert indigène Anolis carolinensis. Les mâles des deux espèces se battent pour le territoire dans leur habitat désormais partagé. Les mâles signalent agressivement en utilisant une série de pompes pour montrer leur condition physique aux autres mâles. Les mâles qui font plus de pompes sont considérés comme plus agressifs que les mâles qui en font moins. Vous vous demandez si les anoles bruns envahissants sont de meilleurs compétiteurs spatiaux que les anoles verts indigènes, et si la compétition spatiale chez ces espèces est liée à leur comportement agressif. Pour tester cela, vous avez transporté des individus capturés à l’état sauvage des deux espèces au laboratoire. Vous avez administré trois tours d’un essai d’agression, dans lequel le lézard a été présenté à un miroir et enregistré. Les mâles perçoivent leur reflet comme un intrus et se livrent à un comportement de démonstration de pompes. Vous avez enregistré le nombre de pompes effectuées lors de chacun des trois essais séparés, puis calculé un niveau d’agression moyenne pour chaque lézard. Vous avez ensuite placé un A. carolinensis indigène et un A. sagrei envahissant dans une arène et enregistré la zone d’espace qu’ils occupaient au cours de trois jours (cm3) dans une variable appelée “utilisation de l’espace”, comme mesure de leur capacité à rivaliser pour l’espace.
Analysez cet ensemble de données pour voir si l’ID de l’espèce ou le niveau d’agression a un effet sur la capacité de compétition spatiale.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=209#h5p-78
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=209#h5p-79
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=209#h5p-80
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=209#h5p-81
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=209#h5p-82
Pour télécharger, cliquez avec le bouton droit de la souris et appuyez sur “Enregistrer le fichier sous” ou “Télécharger le fichier lié”.
Travail non publié – Candidat au doctorat Brendan McEwen
Farrell, W. J., & Wilczynski, W. (2006). Aggressive experience alters place preference in green anole lizards, Anolis carolinensis. Animal Behaviour, 71(5), 1155-1164.
Rodríguez, C., Fusani, L., Raboisson, G., Hödl, W., Ringler, E., & Canoine, V. (2022). Androgen responsiveness to simulated territorial intrusions in Allobates femoralis males: evidence supporting the challenge hypothesis in a territorial frog. General and comparative endocrinology, 326, 114046.
Vous êtes un(e) sociobiologiste qui étudie la base génétique de la sociabilité chez les mouches à fruits. Une étude de dépistage génétique a identifié plusieurs “gènes candidats” qui pourraient jouer un rôle dans la régulation du comportement social chez Drosophila melanogaster. Vous décidez d’étudier le gène candidat Sec5, en réalisant une expérience de knockdown. Des cohortes de mouches mâles et femelles ont été soumises à l’interférence par ARN, éliminant ainsi l’activité du gène Sec5 chez ces individus. Une autre cohorte non modifiée génétiquement de mâles et de femelles a été conservée comme témoin. Vous avez rassemblé des groupes de mouches du même sexe dans des arènes de sociabilité, et vous avez suivi leur comportement d’agrégation dans le temps. Un “indice de sociabilité” a été calculé pour chaque groupe, des scores plus élevés indiquant que les mouches étaient plus étroitement regroupées les unes avec les autres – un signal plus fort de regroupement social.
Analysez cet ensemble de données pour voir si les mâles et les femelles diffèrent dans leurs niveaux de sociabilité, et si le silence du gène Sec5 a affecté la sociabilité chez les mâles ou les femelles
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=211#h5p-83
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=211#h5p-84
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=211#h5p-85
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=211#h5p-86
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=211#h5p-87
Pour télécharger, cliquez avec le bouton droit de la souris et appuyez sur “Enregistrer le fichier sous” ou “Télécharger le fichier lié”.
Cognitive Ecology Lab, Dr. Reuven Dukas, Département de psychologie, neurosciences et comportement de l’Université McMaster https://psych.mcmaster.ca/dukas/index.htm
Torabi-Marashi, A. (2023). Investigating the genetic basis of natural variation in sociability within Drosophila melanogaster (Doctoral dissertation)
Scott, A. M., Dworkin, I., & Dukas, R. (2022). Evolution of sociability by artificial selection. Evolution, 76(3), 541-553
En tant qu’écologiste comportemental à l’Institut de recherche Hamilton, vous vous plongez dans la dynamique sociale intéressante de Neolamprologus pulcher, le poisson cichlidé vivant en groupe originaire du lac Tanganyika en Afrique. Votre objectif principal est d’explorer l’impact du rang social sur les capacités d’apprentissage au sein des groupes de N. pulcher. Dans cette étude captivante, chaque unité sociale de N. pulcher comprend deux reproducteurs dominants et un nombre variable d’aides subordonnés, atteignant souvent jusqu’à 20 individus. Votre recherche se déroule à travers une série de trois expériences, toutes documentées dans un ensemble de données complet. L’ensemble de données englobe des variables clés, y compris l’ID du poisson, le sexe, la taille et trois aspects critiques de l’apprentissage :
Apprentissage initial (Expérience 1) : Les poissons ont été individuellement formés pour déplacer un disque coloré (bleu) pour découvrir une source de nourriture cachée. Les données sont dans la colonne “LearnedInitial”.
Apprentissage associatif (Expérience 2) : Un deuxième disque, de couleur jaune et immobile, a été introduit pour évaluer la capacité du poisson à l’associer à la nourriture. Les données sont dans la colonne “LearnedAssos”.
Apprentissage inversé (Expérience 3) : Dans cette expérience, la couleur du disque qui pouvait être déplacé a été changée, mettant au défi le poisson d’adapter et d’inverser leur comportement appris. Les données sont dans la colonne “LearnedReverse”.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=213#h5p-88
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=213#h5p-89
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=213#h5p-90
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=213#h5p-91
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=213#h5p-92
En tant que chercheur étudiant les habitudes alimentaires des gobies ronds juvéniles (Neogobius melanostomus) dans le port de Hamilton, vous vous plongez dans les subtilités de leur comportement alimentaire, de jour comme de nuit. Le goby rond, un petit poisson d’eau douce originaire d’Eurasie, s’est établi dans diverses régions d’Amérique du Nord, y compris les Grands Lacs. Ces gobies, connus pour leur appétit vorace et leur adaptabilité, jouent un rôle significatif dans les écosystèmes locaux en tant que prédateurs et proies.
Dans le port de Hamilton, les gobies ronds juvéniles se nourrissent principalement de deux types d’organismes : les cladocères et les rotifères. Votre ensemble de données offre des informations précieuses sur le contenu de l’estomac de ces juvéniles, révélant leurs habitudes de consommation à différents moments de la journée. Les variables enregistrées comprennent l’ID du poisson, l’heure de la collecte, et les quantités de cladocères et de rotifères trouvées dans l’estomac de chaque poisson.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=215#h5p-93
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=215#h5p-94
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=215#h5p-95
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=215#h5p-96
Dans cette expérience, les chercheurs ont étudié le comportement de dispersion du gobie rond dans un environnement de laboratoire contrôlé, explorant comment il varie sous des conditions de jour et de nuit. De plus, les niveaux d’activité du gobie ont été enregistrés dans le réservoir expérimental. Chaque gobie a été catégorisé en fonction de sa taille (Petit, Moyen ou Grand) et s’il a montré un comportement de dispersion. Le niveau d’activité de chaque gobie a également été mesuré. L’ensemble de données comprend des informations cruciales sur la taille de chaque gobie, leur comportement de dispersion et leurs niveaux d’activité dans l’environnement expérimental.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=217#h5p-97
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=217#h5p-98
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=217#h5p-99
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=217#h5p-100
Enquêtant sur la dynamique de la population du gobie rond (Neogobius melanostomus) dans le lac Ontario, nous nous penchons sur les caractéristiques biologiques des individus échantillonnés dans ce lac. L’ensemble de données comprend des détails tels que le sexe, la longueur et la masse du poisson, essentiels pour comprendre la démographie de cette espèce envahissante. En analysant ces attributs, nous visons à obtenir des informations sur la distribution, les modèles de croissance et les impacts potentiels du gobie rond dans l’écosystème du lac.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=219#h5p-101
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=219#h5p-102
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=219#h5p-103
Dans notre étude, nous étudions le comportement de nage des gobies ronds juvéniles (Neogobius melanostomus) à l’aide d’une expérience de tunnel de nage. Cet environnement contrôlé nous permet d’observer deux comportements principaux : la nage active, caractérisée par un mouvement et une exploration continus, et le maintien en station, où les poissons maintiennent une position relativement stationnaire. En enregistrant ces comportements, nous visons à comprendre les modèles d’activité et les préférences du gobie rond en réponse à des conditions variables. Notre ensemble de données comprend des mesures des durées de nage et de maintien, ainsi que la catégorisation de la taille des poissons, fournissant des informations sur leur dynamique locomotrice et leurs interactions écologiques.
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=221#h5p-104
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=221#h5p-105
An interactive H5P element has been excluded from this version of the text. You can view it online here:
https://ecampusontario.pressbooks.pub/rspnc/?p=221#h5p-106
1
Tous les fichiers de données référencés dans ce REL sont disponibles sur la page GitHub à l’adresse suivante : https://github.com/HashemiScience/data4pnb/